
Georges Honos, M.D., FRCPC, FACC
Professeur agrégé de médecine
Université de Montréal
Chef, Cardiologie
Directeur du programme CV
Centre Hospitalier de l’Université de Montréal (CHUM)
Simon Kouz, M.D., FRCPC, FESC, FACC
Professeur de clinique,
Université Laval
Chef, Médecine
Chef, Cardiologie
Directeur
Unité de recherche en cardiologie
Centre hospitalier régional de Lanaudière
Le traitement anticoagulant est utilisé avec beaucoup de succès depuis des décennies pour la prévention de l’AVC chez les patients qui souffrent de fibrillation auriculaire (FA). Ces quelques dernières années, l’arsenal thérapeutique s’est considérablement enrichi avec l’ajout d’anticoagulants qui agissent en empruntant de nouvelles voies.
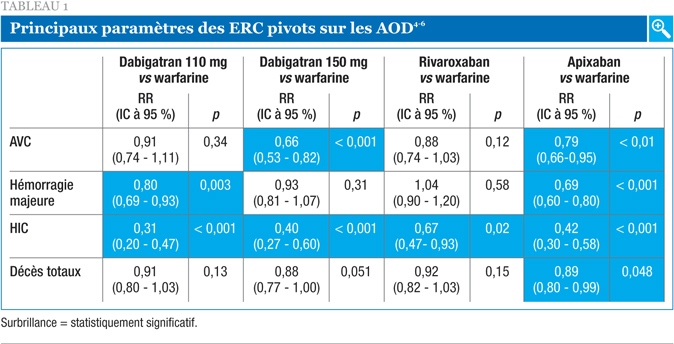
Les nouveaux agents actuellement disponibles sont l’apixaban et le rivaroxaban (tous deux des inhibiteurs oraux directs du facteur Xa) et le dabigatran (un inhibiteur oral direct de la thrombine)1-3. L’approbation de ces anticoagulants oraux directs (AOD) repose sur des essais cliniques majeurs ayant clairement démontré une réduction plus marquée des risques d’AVC et/ou d’hémorragies majeures comparativement à la warfarine. Le Tableau 1 résume les paramètres clés des principaux essais à répartition aléatoire et contrôlés (ERC) qui ont porté sur ces AOD4-6. Lors de ces études, l’apixaban et le dabigatran à 150 mg chacun ont signifi-cativement réduit le risque d’AVC, tandis que l’apixaban et le dabigatran à 100 mg ont réduit le risque d’hémorragie majeure comparativement à la warfarine. Aux doses étudiées, ces trois nouveaux agents ont réduit le risque d’hémorragie intracrânienne (HIC). En terminant, l’apixaban a réduit le risque global de mortalité.
Il n’est pas possible d’appliquer à tous les patients les résultats obtenus lors de ces ERC sur les AOD, étant donné que le protocole strict des ERC génère des renseignements exclusifs à un spectre relativement étroit de patients. Pour tenir compte des variables de confusion, les ERC assujettissent leur recrutement à un ensemble de critères préspécifiés qui ne reflètent pas nécessairement le profil de tous les patients susceptibles de bénéficier de ces agents.
La recherche se poursuit à partir des bases de données des ERC pour tenter de mieux identifier les sous-groupes de patients pouvant bénéficier ou non de chacun des agents. Lors du Congrès annuel de la Société européenne de cardiologie à Londres en 2015 (ESC 2015, du 29 août au 2 septembre), plusieurs présentations et affiches ont porté sur ce type de données.
Encore plus important à noter peut-être, à mesure que ces agents sont davantage utilisés dans la pratique, de nouvelles données significatives émergent au sujet des AOD et de leur utilisation courante. C’est ce que révèle l’examen de bases de données plus volumineuses qui incluent des patients traités au moyen de ces médicaments dans des contextes cliniques moins strictement restreints que les ERC. On y retrouve des registres ciblés, des études d’observation et des analyses de bases de données administratives de systèmes de santé. Au Congrès ESC 2015, une foule de renseignements ont été présentés à partir de ces types de sources. Dans bien des cas, ces nouvelles données confirment les conclusions clés des ERC : c’est-à-dire que les trois agents actuellement disponibles réduisent efficacement le risque d’AVC chez les patients atteints de FA, qu’ils ne sont pas dépourvus de risques et qu’ils semblent présenter des différences cliniquement significatives entre eux.
Le rapport qui suit résume les points saillants des données tirées de registres et autres bases de données de pharmacovigilance postcommercialisation présentées au Congrès ESC 2015. Suivra une discussion des répercussions de ces observations, y compris en quoi elles étayent les données des ERC et quel impact elles peuvent avoir sur la pratique clinique au Canada.
ESC 2015 : Ce que révèlent les registres d’utilisation dans la pratique et d’autres données de pharmacovigilance postcommercialisation
Risques hémorragiques associés aux AOD dans la pratique (analyse des bases de données de réclamations américaines). L’un des ensembles de données les plus éloquents présentés au Congrès ESC 2015 reposait sur une comparaison du risque hémorragique dans la pratique chez des patients souffrant de FA non valvulaire traités par AOD7. Les analyses de cette étude portaient sur une volumineuse base de données sur les soins de santé aux États-Unis (réclamations d’assurance MarketScan Earlyview). Les investigateurs ont recensé plus de 60 000 patients adultes (âgés de 18 ans ou plus) ayant reçu une première anticoagulothérapie par AOD ou étant passés de la warfarine à un AOD en 2013 et en 2014. Cela incluait 8 785 patients traités par apixaban, 20 963 traités par dabigatran et 30 529 traités par rivaroxaban.
Pour cette analyse, les patients ont été suivis pendant une période allant jusqu’à six mois ou jusqu’à ce qu’ils fassent une hémorragie, qu’ils arrêtent/changent de médicament ou quittent l’étude. Les principaux paramètres étudiés étaient : hémorragie majeure et hémorragie non majeure cliniquement pertinente (NMCP).
L’âge moyen des individus de la base de données était similaire entre les trois groupes traités, même s’il y avait significativement moins de patients de 75 ans et plus dans le groupe sous rivaroxaban (34,5 %, contre 38,1 % pour l’apixaban et
38,0 % pour le dabigatran). La proportion de patients passés de la warfarine à un des nouveaux agents se répartissait comme suit : 17,3 % du groupe sous apixaban, 15,7 % du groupe sous rivaroxaban et 4,4 % du groupe sous dabigatran. Parmi les autres différences, mentionnons une proportion plus élevée d’utilisateurs d’antiplaquettaires, une proportion plus élevée de comorbidités et des scores CHA2DS2VASc et HAS-BLED légèrement plus élevés dans le groupe sous apixaban comparativement aux sujets sous dabigatran ou rivaroxaban.
La Figure 1 montre la comparaison des risques hémorragiques entre les groupes sous apixaban et dabigatran, en tenant compte de l’âge, du sexe, des comorbidités et de l’utilisation de médicaments. Si la plupart des paramètres étaient similaires, on note que le risque d’hémorragie GI était significativement plus faible avec l’apixaban qu’avec le dabigatran.
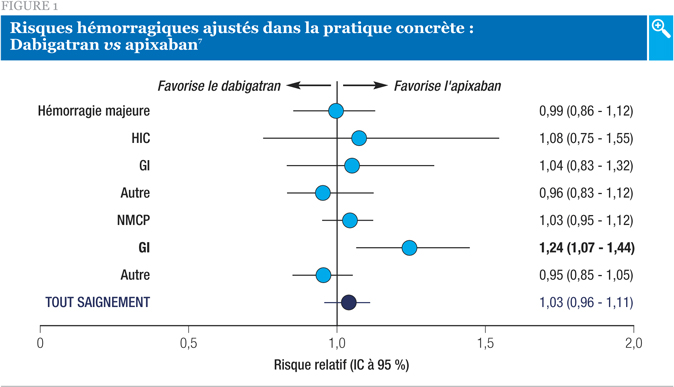
La comparaison entre l’apixaban et le rivaroxaban est illustrée à la Figure 2. Dans cette analyse, le risque ajusté de chaque type différent d’hémorragie était significativement plus élevé avec le rivaroxaban. Cela inclut un risque de 34 % plus élevé d’hémorragie majeure (risque relatif [RR] 1,34, intervalle de confiance [IC] à 95 % 1,20 – 1,51) et un risque plus élevé de 39 % d’hémorragie NMCP (RR 1,39, IC à 95 % 1,28 – 1,51).
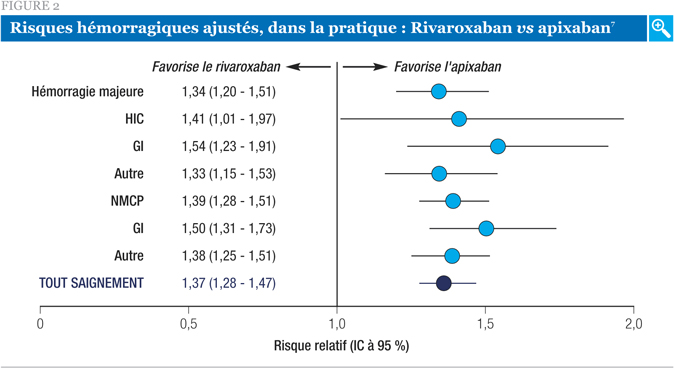
Si les investigateurs ont convenu que l’étude des bases de données de réclamations comportait des limites (notamment le risque de données manquantes ou d’imprécisions quant au moment du début des traitements et le fait que certaines variables de confusion potentielles ne soient pas mesurées), ils ont conclu que le rivaroxaban semble comporter un risque accru d’hémorragie majeure et NMCP comparativement aux autres AOD au cours des six premiers mois suivant l’instauration du traitement.
Plusieurs autres analyses rétrospectives de moindre envergure portant sur les trois mêmes AOD ont aussi été présentées. Elles incluaient une analyse des données provenant d’une autre base de données américaine, IMS PharMetrics8. La population se composait de
9 150 patients adultes souffrant de FA non valvulaire qui n’avaient encore jamais pris d’anticoagulants oraux et venaient de commencer un traitement par AOD8.
Comme ce fut le cas avec l’analyse plus volumineuse décrite précédemment, les investigateurs ont signalé que le risque d’hémorragie majeure était significativement plus élevé avec le rivaroxaban qu’avec l’apixaban et qu’il n’y avait pas de différence entre le dabigatran et l’apixaban pour ce qui est de ce paramètre. Le nombre d’hospitalisations de toutes causes s’est révélé significativement plus élevé avec le rivaroxaban et le dabigatran qu’avec l’apixaban, avec des RR de 1,57 et 1,37, respectivement8. De plus, les coûts des soins de santé de toutes causes ont été substantiellement moindres avec l’apixaban qu’avec le rivaroxaban ou le dabigatran (Figure 3)8.
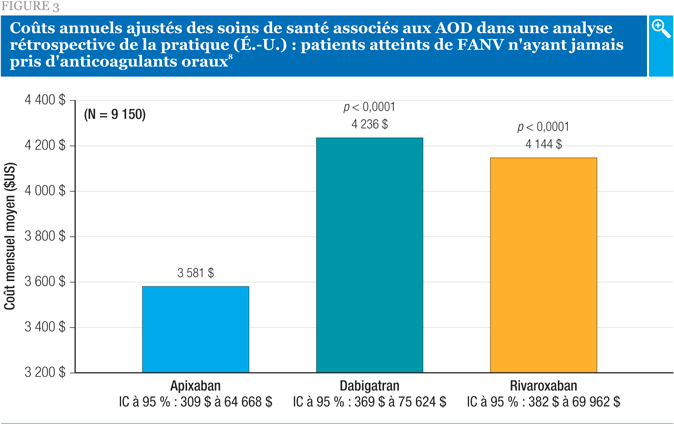
Ces données pharmacoéconomiques ont trouvé écho dans une étude du Royaume-Uni selon laquelle l’apixaban a semblé être un traitement plus efficace que la warfarine ou le dabigatran, à un coût économiquement accepté9.
D’autres analyses ont aussi montré le même type de risque associé aux AOD lors d’une utilisation dans la pratique, avec des taux hémorragiques moindres associés à l’apixaban et au dabigatran par rapport au rivaroxaban ou à la warfarine10-12.
Le point sur le registre GARFIELD-AF et ses données initiales. Le registre GARFIELD-AF est une initiative de recherche universitaire indépendante regroupant des sites représentatifs de la pratique à l’échelle nationale en ce qui concerne la FA dans 35 pays, dont le Canada10. Au moment de sa présentation au Congrès ESC 2015, environ 45 000 patients avaient été inscrits, sur un objectif total de 57 00013.
La majorité de la population de ce registre sera une population de patients non sélectionnés, inscrits de manière prospective moins de huit semaines après un diagnostic de FA. En plus de la FA, les patients ont au moins un autre facteur de risque d’AVC, déterminé par l’investigateur. Il n’y a pas de critères d’admissibilité en ce qui concerne les scores de risques préexistants. En plus des patients prospectifs, l’étude comptera une minorité non négligeable (d’environ
5 000 patients) inscrite rétrospectivement dans les 6 à 24 mois suivant le diagnostic. Les sujets seront répartis en cinq cohortes séquentielles selon la date du diagnostic. Le recrutement devrait être terminé d’ici l’été 2016 et les analyses finales prévues devraient être dévoilées d’ici l’été 2018. Selon l’année d’inscription d’un patient donné, le suivi prévu sera d’au moins deux ans et d’au plus huit ans.
À ce jour, des données de référence évaluables sont disponibles pour environ
39 670 patients, des mesures paramétriques à un an, pour 28 624 patients et des mesures paramétriques à deux ans, pour 17 162 patients10.
L’étude GARFIELD-AF a fourni des données sur l’utilisation croissante des AOD avec le temps. Dans la première cohorte de l’étude (diagnostic posé en 2010-2011), 4,2 % des patients se sont fait prescrire un AOD. La proportion a progressivement augmenté dans les cohortes subséquentes, la quatrième (diagnostic posé en 2014-2015) comptant 37,0 % de patients traités par AOD au départ13. Globalement, l’utilisation de tout type d’anticoagulant a aussi augmenté, passant de 57,4 % à 71,1 % entre la première et la quatrième cohorte.
Les analyses prospectives effectuées sur les données du registre portent entre autres sur le taux d’AVC/embolies systémiques (ES), d’hémorragies majeures et de mortalité de toutes causes; les types d’AVC/ES et d’événements hémorragiques majeurs et leur gravité; les causes de mortalité et la détermination des variables associées à ces événements.
Les données présentées au Congrès ESC 2015 incluent les données sur les paramètres principaux à deux ans pour les cohortes 1 et 213,14, une analyse des différences régionales de cette base de données globale15 et l’impact sur les paramètres de facteurs tels que : sexe16, comorbidités16,17 et temps passé dans l’éventail des taux thérapeutiques18.
Pour l’analyse à deux ans des cohortes 1 et 2 (n = 17 162), l’âge moyen des patients était d’environ 70 ans; 38 % de tous les sujets avaient ≥ 75 ans. Les comorbidités étaient fréquentes : 78,1 % des sujets souffraient d’hypertension, 22 % de diabète, 20,6 % d’insuffisance cardiaque congestive, 15 % de maladie vasculaire (maladie artérielle périphérique ou coronaropathie avec antécédents de syndrome coronarien aigu), 13 % avaient des antécédents d’AVC et 10 % d’insuffisance rénale chronique (de grade 3 ou plus)14.
Les taux d’événements (AVC, hémorragie majeure, mortalité de toutes causes) ont été les plus élevés au cours de la première année suivant le diagnostic, les taux étant moindres au cours de la seconde année (Figure 4)13,14. Le décès a été l’événement majeur le plus fréquent au cours de la période d’observation, les taux d’AVC et d’hémorragie majeure ayant été considérablement moindres. La mortalité a été attribuée à des causes cardiovasculaires (CV) dans 53 % des cas.
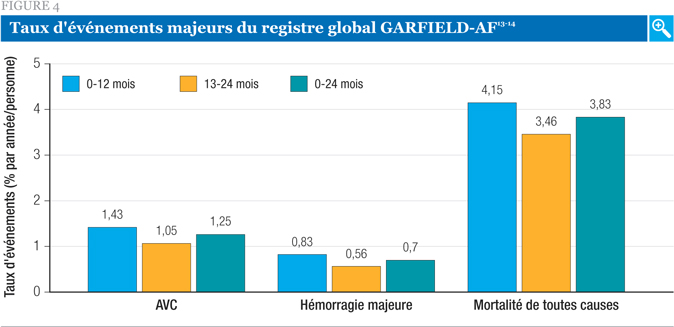
Les AVC observés dans cet ensemble étaient principalement ischémiques (n = 260). On a aussi dénombré 37 AVC hémorragiques et 68 AVC de type inconnu.
L’utilisation de l’anticoagulothérapie a été associée à des réductions significatives du risque d’AVC et de mortalité de toutes causes. On a noté une augmentation du nombre d’hémorragies associées à l’anticoagulothérapie (vs aucune), mais cela ne s’est pas révélé statistiquement significatif. Parmi les autres facteurs analysés, l’âge a été plus étroitement associé au risque de décès, d’AVC/ES et d’hémorragies majeures14. Les scores de risque plus élevés (scores CHA2DS2VASc ou HAS-BLED) ont aussi été clairement associés à un risque accru d’événements14. La présence d’insuffisance rénale a aussi été en lien avec un risque accru à l’égard des trois principaux types d’événements14,17,18.
En ce qui a trait au sexe, les femmes avaient quatre ou cinq ans de plus que les hommes au départ et une proportion plus élevée de femmes étaient âgées de 75 ans ou plus (47 % vs 30 % des hommes)16. La maladie vasculaire était plus fréquente chez les hommes (17,7 % vs 11,9 %), tout comme les antécédents de tabagisme (50,1 % vs 15,9 %)16. Après un an, les taux d’événements se sont révélés plus élevés chez les femmes que chez les hommes : les taux d’AVC/ES étaient de 1,62 % par année-personne chez les femmes et de 1,17 % chez les hommes, l’hémorragie majeure, de 0,93 % vs 0,79 % et la mortalité de toutes causes, de 4,48 % vs 4,04 %.
L’effet de l’anticoagulothérapie sur la réduction du risque a aussi été significativement et substantiellement plus marqué chez les hommes que chez les femmes pour chacun des paramètres AVC/ES, hémorragie majeure et mortalité de toutes causes.
L’analyse des comorbidités a révélé que les taux d’événements étaient plus élevés chez les sujets qui avaient des antécédents d’insuffisance rénale chronique (IRC) ou d’infarctus du myocarde (IM) ou qui avaient plus de 80 ans. Les auteurs en ont conclu qu’il faudrait envisager de prescrire plus souvent des anticoagulants chez les patients atteints de FA en présence de telles comorbidités17.
En ce qui concerne le temps passé à l’intérieur de l’éventail des valeurs thérapeutiques avec les anticoagulants classiques (antivitamine K ou AVK), les conclusions de l’étude GARFIELD-AF appuient celles d’analyses antérieures selon lesquelles le temps passé à l’intérieur des valeurs thérapeutiques et la fréquence sont prédictifs des paramètres majeurs19.
Caractéristiques et observations du registre GLORIA-AF. Le registre GLORIA-AF est un autre registre global d’observation qui prévoit suivre
56 000 patients inscrits auprès d’environ 1 000 centres répartis entre 44 pays20.
Les sujets sont des patients adultes porteurs d’un diagnostic récent (< trois mois) de FA non valvulaire et présentant au moins un autre facteur de risque d’AVC (score CHA2DS2VASc ≥ 1).
Les objectifs sont de caractériser cette population de patients « réels » et d’étudier les modes de présentation, les prédicteurs et les résultats associés à divers schémas thérapeutiques antithrombotiques pour la prévention de l’AVC20.
Les données disponibles au moment du Congrès ESC 2015 provenaient de la
phase II préplanifiée du registre en prévision de l’approbation du premier AOD, le dabigatran. La phase I était une analyse transversale réalisée avant l’approbation des AOD et des analyses de phase III sont prévues, en l’occurrence, quand il est possible de comparer les caractéristiques de départ des patients traités par AOD et AVK20.
Parmi les 15 092 patients recrutés à la phase II, les contextes de soins incluaient : hôpitaux universitaires (32,2 %), bureaux de spécialistes (30 %), hôpitaux communautaires (14,5 %) et cliniques de médecine familiale (11,3 %)20.
La plupart des caractéristiques de départ étaient similaires à celles du registre GARFIELD-AF : âge médian 71,0 ans, 74,6 % ayant des antécédents d’hypertension, 24,2 % des antécédents d’insuffisance cardiaque congestive, 10,5 % d’AVC, 10,6 % d’IM. La plupart des patients présentaient un score de risque CHADS2 modéré (score = 1; 34,1 % des patients) ou élevé (score ≥ 2; 57,8 % des patients).
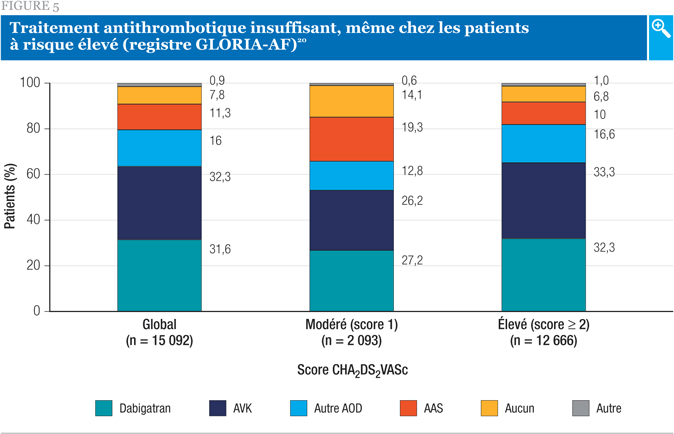
Parmi les patients de la phase II, une forte proportion utilisait des anticoagulants au départ, une proportion plus grande étant traitée par AOD (47,6 %) plutôt que par AVK (32,3 %; Figure 5). À noter toutefois, une minorité substantielle de patients ne recevait aucun anticoagulant, même dans le groupe à risque élevé20. Une analyse plus détaillée de cette cohorte a révélé que même dans le sous-groupe d’individus à risque très élevé ayant déjà fait un AVC, le seul traitement antithrombotique était un antiplaquettaire chez 10,8 % des patients, tandis que 5,8 % ne recevaient absolument aucun traitement antithrombotique21. Une autre analyse a révélé que malgré le risque hémorragique accru associé au traitement associatif, environ 5 % à 7 % des patients du registre recevaient un antiplaquettaire en plus d’un anticoagulant22.
Résultats de l’étude XANTUS sur le rivaroxaban. XANTUS est une étude prospective d’observation qui mesurait l’innocuité et l’efficacité du rivaroxaban utilisé dans la pratique de routine pour la FA non valvulaire23,24. L’étude a regroupé 6 784 patients traités par rivaroxaban dans 311 centres en Europe, en Israël et au Canada. La durée moyenne du traitement par rivaroxaban a été d’environ un an.
Les principaux résultats de l’étude présentés au Congrès ESC 2015 ont été les suivants : les hémorragies majeures associées au traitement sont survenues à un taux de 2,1 événements par 100 années-patients, tandis que le taux de mortalité globale a été de 1,9 par 100 années-patients. Les AVC ont été moins fréquents, soit un taux de 0,7 événement par 100 années-patients23,24.
Analyses des résultats selon la conformité aux lignes directrices (registre EORP-AF). Le registre EORP-AF est un programme européen en cours qui regroupe 2 634 patients souffrant de FA provenant de neuf pays, tous sous les soins de cardiologues25,26.
L’objectif de cette analyse présentée au Congrès ESC 2015 était d’évaluer les paramètres (décès, thrombo-embolie [TE], hémorragie et paramètres mixtes regroupant TE, décès CV ou hémorragie) en fonction de la conformité aux lignes directrices de l’ESC 2012 pour la FA. Les investigateurs ont classifié les schémas thérapeutiques des patients comme suit : conformes aux lignes directrices, traitement insuffisant ou surtraitement.
Comme l’illustre la Figure 6, le taux de TE et du paramètre mixte ont été plus bas chez les sujets dont le traitement était conforme aux lignes directrices. Des paramètres significativement plus favorables ont été observés sur le plan de la mortalité et de la TE, de même que sur le plan du paramètre mixte mortalité CV et toute TE ou hémorragie.
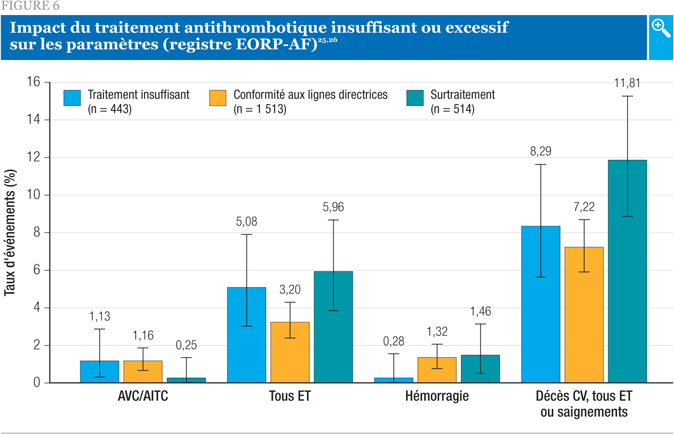
Les auteurs ont conclu à l’importance de ces résultats compte tenu que les lignes directrices de 2012 préconisent une approche qui permet d’offrir l’anticoagulothérapie à quiconque présente au moins un facteur de risque plutôt que de la réserver aux patients à risque élevé (comme le stipulaient les lignes directrices antérieures).
Évaluation de la fidélité au traitement par apixaban dans la pratique (étude AEGEAN). Une autre étude de pharmacovigilance postcommercialisation présentée au Congrès ESC 2015 a exploré l’impact d’un programme d’enseignement aux patients sur les taux d’observance thérapeutique et de maintien du traitement par apixaban27. Cette étude à répartition aléatoire a assigné plus de 1 000 patients soit à l’apixaban et aux soins standard, soit à l’apixaban et à un programme d’enseignement structuré. Ce programme incluait une brochure additionnelle pour expliquer la FA et le traitement anticoagulant aux patients, des outils de rappel (porte-clés, service de messages d’alerte ou applications pour appareils mobiles) et accès à une clinique virtuelle nationale desservie par le personnel des cliniques d’anticoagulothérapie existantes.
À 24 semaines, les taux d’observance thérapeutique et de maintien des traitements étaient élevés dans les deux groupes (soins standard : observance thérapeutique 88,5 % et persistance 90,5 %; programme d’enseignement : observance thérapeutique 88,3 % et persistance 91,1 %) sans différence significative entre les groupes. Aucun prédicteur significatif de l’observance thérapeutique n’a émergé de l’analyse des sous-groupes préspécifiés.
Réflexions sur les essais cliniques à répartition aléatoire
Même des années après la publication des ERC, on voit encore des résultats fascinants en provenance de ces études de référence. Par exemple, dans des sous-analyses de l’essai ARISTOTLE qui comparait l’apixaban à la warfarine, l’hémorragie NMCP a affecté 14,2 % des patients traités par warfarine, contre
10,1 % des patients traités par apixaban (réduction du risque de 32 % avec l’apixaban)28.
L’effet de l’anticoagulothérapie sur la fonction rénale a aussi été évalué dans l’étude ARISTOTLE29. Globalement, le taux de filtration glomérulaire estimé (TFGe) médian a légèrement diminué à un rythme de 0,6 mL/min par année. Indépendamment du TFGe, l’apixaban a été associé à un risque moindre d’événements comparativement à la warfarine.
Les investigateurs ont aussi utilisé les données de l’étude ARISTOTLE pour analyser l’impact de l’apixaban vs warfarine chez les patients qui ne présentaient aucun critère de réduction de la dose d’apixaban (de 5 mg à 2,5 mg) et chez ceux qui présentaient un critère (âge ≥ 80 ans, créatinine ≥ 133 µmol/L [≥ 1,5 mg/dL], poids ≤ 60 kg)30. Une réduction de dose est recommandée si un patient présente deux de ces critères. Les investigateurs ont signalé que les bienfaits de l’apixaban à 5,0 mg vs warfarine étaient similaires pour ceux qui présentaient un critère et ceux qui n’en présentaient aucun, rappelant l’innocuité et l’efficacité de cette dose chez les patients qui ne présentent qu’un seul critère.
Les données des ERC ont aussi servi à réaliser une comparaison indirecte des paramètres AVC et hémorragie majeure associés à l’apixaban (étude ARISTOTLE) ou au rivaroxaban (étude ROCKET-AF)31. À l’aide d’une méthode de comparaison indirecte ajustée (MAIC, Matching Adjusted Indirect Comparison) appliquée aux données relatives aux patients de ces études, on a observé un risque significativement plus faible d’hémorragies majeures avec l’apixaban qu’avec le rivaroxaban (RR 0,75, IC à 95 % 0,67–82) et un risque limite d’AVC/ES significativement moindre (RR 0,88, IC à 95 % 0,80–1,00).
Les données de l’étude ARISTOTLE ont aussi servi à générer un score de risque en fonction des biomarqueurs pour les patients atteints de FA (score de risque
d’AVC « ABC »), dont la validation a été présentée au Congrès ESC 201532. Ce nouvel outil s’est révélé plus performant que le score CHA2DS2VASc pour plusieurs populations touchées par la FA et on peut recommander son utilisation dans la pratique clinique.
Discussion
Les données présentées au Congrès ESC 2015, particulièrement en ce qui concerne les études sur les données provenant des registres et de la pharmacovigilance postcommercialisation concernant les AOD, constituent un complément d’information intéressant qui étayent les ERC que nous connaissions déjà.
La comparaison des paramètres pour chacun des AOD est intéressante, puisque la définition variable du paramètre hémorragique entre les différents ERC ne permet pas de faire des comparaisons transversales. Même si les données des registres et autres données tirées de la pratique s’accompagnent de biais de sélection, etc., elles peuvent rassurer les médecins et leurs patients sur le fait que les résultats des ERC sont étayés. De plus, étant donné la taille des échantillons de populations étudiées, elles pourraient aussi permettre la découverte d’effets indésirables rares liés aux traitements qui ne sont pas mis au jour par les ERC.
Toutefois, ces types de registres sont conçus pour détecter des effets imprévus que n’auraient pas détectés les ERC, et en dresser ainsi un tableau plus complet. Les registres peuvent aider à confirmer les observations des essais. En même temps, les patients des essais sont également de vrais patients, et dans les registres, il n’y a pas de comparateurs.
Pour ce qui est des différences entre les trois AOD, les données tirées de la pratique appuient les résultats des principaux ERC en ce qui a trait aux événements hémorragiques. Dans les ERC, l’apixaban et le dabigatran ont été associés à des réductions substantielles et significatives du risque hémorragique par rapport à la warfarine, y compris les hémorragies majeures, tandis que le rivaroxaban n’a pas été associé à une réduction significative des hémorragies majeures. Dans les analyses des bases de données, l’apixaban et le dabigatran se sont révélés grosso modo similaires, alors qu’on a observé des différences majeures et significatives favorisant l’apixaban plutôt que le rivaroxaban ou la warfarine en ce qui concerne les catégories hémorragiques. Cette observation est importante pour les médecins : la commodité (p. ex. celle du rivaroxaban) ne signifie pas nécessairement qu’un médicament est meilleur ou plus sécuritaire. Malheureusement, aucune comparaison des résultats obtenus avec les divers AOD dans les registres plus volumineux (p. ex. GARFIELD-AF, GLORIA-AF) n’a été présentée au Congrès ESC 2015 ce qui leur aurait donné plus de poids. On attend impatiemment ce type de résultats.
Il est également important d’observer que l’apixaban est économique par rapport aux autres AOD (selon deux groupes distincts d’auteurs utilisant des ensembles de données différents). Ces médicaments sont considérés plus coûteux que la warfarine et pour maximiser les bienfaits potentiels des AOD sur le plan de l’efficacité et de l’innocuité pour le plus grand nombre possible de patients candidats à ce type de traitement, des choix économiques devront être faits.
À cet égard, il faut encore noter que la warfarine demeure un outil utile dans l’arsenal thérapeutique pour réduire le risque d’AVC comparativement à l’absence d’anticoagulothérapie. Par contre, pour être utile, le temps passé à l’intérieur des valeurs thérapeutiques doit se maintenir à 65 % ou plus.
Le fait que de nombreux patients soient traités par antiplaquettaires et anticoagulothérapie, comme on le voit dans les bases de données GARFIELD-AF et GLORIA-AF, est une autre importante observation. L’utilisation d’antiplaquettaires est recommandée pour certaines comorbidités qui accompagnent parfois la FA
(p. ex. post-IM, maladie artérielle périphérique), mais il faut reconnaître le risque hémorragique additionnel lié à de telles associations. La décision d’instaurer ou de continuer concomitamment plusieurs antithrombotiques doit être prise au cas par cas par des spécialistes qui connaissent bien les comorbidités et le risque CV global de leurs patients.
Plusieurs études actuellement en cours sur les traitements antithrombotiques d’association permettront de clarifier le rôle des anticoagulants et des antiplaquettaires administrés concomitamment chez des patients atteints de FA et de coronaropathie (p. ex. AUGUSTUS, PIONEER AF-PCI et RE-DUAL PCI).
Un autre thème intéressant abordé dans ce compte-rendu est le suivant : une réduction de dose d’apixaban ne semble pas être nécessaire chez les patients qui ne présentent qu’un seul facteur de risque. Les médecins doivent tenir compte de ces observations puisqu’une FA insuffisamment traitée est associée à un pronostic plus défavorable.
En terminant, selon une autre observation clé tirée du Congrès ESC 2015, même les patients à risque élevé qui ont déjà subi un AVC ne reçoivent peut-être pas d’anticoagulothérapie. Cela rappelle la nécessité d’observer les lignes directrices fondées sur des preuves et de traiter les patients en conséquence pour optimiser les bienfaits des traitements actuellement disponibles.
Références
1. Bristol-Myers Squibb Canada. Monographie d’Eliquis. Révisée le 11 août 2015.
2. Bayer Inc. Monographie de Xarelto. Révisée le 20 juillet 2015.
3. Boehringer Ingelheim Canada Ltd. Monographie de Pradaxa. Révisée le 5 juin 2015.
4. Connolly SJ, Ezekowitz MD, Yusuf S, et coll. Dabigatran vs. warfarin in patients with atrial fibrillation. N Engl J Med 2009; 361:1139-51.
5. Patel MR, Mahaffey KW, Garg J, et coll. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med 2011; 365:883-91.
6. Granger CB, Alexander JH, McMurray JJ, et coll. Apixaban vs. warfarin in patients with atrial fibrillation. N Engl J Med 2011; 365:981-92.
7. Lip GY, Tepper P, Mardekian J, et coll. Real-world comparison of bleeding risks among non-valvular atrial fibrillation patients on apixaban, dabigatran, rivaroxaban: cohorts comprising new initiators and/or switchers from warfarin. Eur Heart J 2015; 36(Supplément au résumé):339; et présenté au Congrès ESC 2015.
8. Deitelzweig S, Bruno A, Tate N, et coll. Major bleeding, hospitalisation rates and healthcare costs among non-valvular atrial fibrillation patients naive to oral anticoagulation and newly treated with novel oral anticoagulants. Eur Heart J 2015; 36(Supplément au résumé):338; et présenté au Congrès ESC 2015.
9. Lip GY, Lanitis T, Kongnakor T, et coll. Comparative cost-effectiveness of oral anticoagulants for stroke prevention in non-valvular atrial fibrillation patients in the UK. Eur Heart J 2015; 36(Supplément au résumé):864; et présenté par affiche au Congrès ESC 2015.
10. Lin I, Masseria C, Mardekian J, et coll. Real-world bleeding risk among non-valvular atrial fibrillation (NVAF) patients prescribed apixaban, dabigatran, rivaroxaban and warfarin: analysis of electronic health records. Eur Heart J 2015; 36(Supplément au résumé):1084; et présenté par affiche au Congrès ESC 2015.
11. Lip GY, Pan X, Kamble S, et coll. Real world comparison of major bleeding risk among non-valvular atrial fibrillation patients newly initiated on apixaban, dabigatran, rivaroxaban or warfarin. Eur Heart J 2015; 36(Supplément au résumé):1085; et présenté par affiche au Congrès ESC 2015.
12. Deitelzweig S, Bruno A, Trocio J, et coll. Early assessment of bleeding-related hospital readmissions among nonvalvular atrial fibrillation patients treated with the new oral anticoagulants using an electronic medical record database in the US. Eur Heart J 2015; 36(Supplément au résumé):1083; et présenté par affiche au Congrès ESC 2015.
13. Kakkar A. Global status of GARFIELD-AF. Anticoagulation and atrial fibrillation (AF): real life data from the GARFIELD-AF Registry. Présenté au Congrès ESC 2015.
14. Bassand J-P. GARFIELD-AF registry: 2-year outcomes data for cohorts 1 and 2. Anticoagulation and Atrial Fibrillation (AF): real life data from the GARFIELD-AF Registry. Présenté au Congrès ESC 2015.
15. Goto S. Regional differences in baseline characteristics, use of antithrombotic therapy and outcomes in newly diagnosed atrial fibrillation: Results from cohorts 1–3 of GARFIELD-AF. Anticoagulation and Atrial Fibrillation (AF): real life data from the GARFIELD-AF Registry. Présenté au Congrès ESC 2015.
16. Camm AJ. Gender and outcomes in cohorts 1–3 of GARFIELD-AF. Anticoagulation and Atrial Fibrillation (AF): real life data from the GARFIELD-AF Registry. Présenté au Congrès ESC 2015.
17. Goldhaber SZ. GARFIELD-AF: Impact of comorbidities on outcomes in cohorts 1–3. Anticoagulation and Atrial Fibrillation (AF): real life data from the GARFIELD-AF Registry. Présenté au Congrès ESC 2015.
18. Goto S, Atar D, Bassand J-P, et coll. Stroke, major bleeding, and mortality in newly diagnosed atrial fibrillation with moderate-to-severe chronic kidney disease: results from GARFIELD-AF. Eur Heart J 2015; 36(Supplément au résumé):987; et présenté au Congrès ESC 2015.
19. Haas S. Time in therapeutic range and frequency in range with 1-year outcomes in cohorts 1–3 of GARFIELD-AF. Anticoagulation and Atrial Fibrillation (AF): real life data from the GARFIELD-AF Registry. Présenté au Congrès ESC 2015.
20. Huisman MV. Global registry on long-term oral antithrombotic treatment in patients with atrial fibrillation: final baseline characteristics of GLORIA-AF Phase II. Présenté au Congrès ESC 2015.
21. Lip GY, Halperin JL, Diener HC, et coll. Use of antithrombotic therapy in patients with atrial fibrillation and prior stroke: insights from the global GLORIA-AF registry. Eur Heart J 2015; 36(Supplément au résumé):243; et présenté par affiche au Congrès ESC 2015.
22. Lip GY, Halperin JL, Diener HC, et coll. Use of oral anticoagulants in combination with antiplatelet therapy: insights from the GLORIA-AF registry. Eur Heart J 2015; 36(Supplément au résumé):235; et présenté par affiche au Congrès ESC 2015.
23. Camm AJ, Amarenco P, Haas S, et coll. XANTUS: a real-world, prospective, observational study of patients treated with rivaroxaban for stroke prevention in atrial fibrillation. Eur Heart J 2015; cyberpublication avant impression, Le 15 septembre; et présenté au Congrès ESC 2015.
24. Camm AJ, Amarenco P, Haas S, et coll. XANTUS: a real-world, prospective, observational study of patients treated with rivaroxaban for stroke prevention in atrial fibrillation. Eur Heart J 2015; cyberpublication avant impression, Le 15 septembre; et présenté au Congrès ESC 2015.
25. Lip G. Improved outcomes with ESC guideline-adherent antithrombotic treatment in high-risk patients with atrial fibrillation. A report from the EORP-AF General Pilot Registry. Présenté au Congrès ESC 2015.
26. Lip GY, Laroche C, Popescu MI, et coll. Improved outcomes with European Society of Cardiology guideline-adherent antithrombotic treatment in high-risk patients with atrial fibrillation: a report from the EORP-AF General Pilot Registry. Europace 2015; [cyberpublication avant impression].
27. Montalescot G, Brotons C, Sosyns B, et coll. Assessment of an education and guidance program for apixaban adherence in non-valvular atrial fibrillation: the randomised AEGEAN study. Présenté au Congrès ESC 2015.
28. Bahit MC, Lopes RD, Wojdyla DM, et coll. Less non-major bleeding with apixaban versus warfarin among patients with atrial fibrillation: insights from the ARISTOTLE trial. Eur Heart J 2015; 36(Supplément au résumé):338-9; et présenté au Congrès ESC 2015.
29. Hijazi Z, Hohnloser SH, Andersson U, et coll. Efficacy and safety of apixaban compared with warfarin in relation to renal function over time in patients with atrial fibrillation: Insights from the ARISTOTLE trial. Eur Heart J 2015; 36(Supplément au résumé):339; et présenté au Congrès ESC 2015.
30. Alexander J, Andersson U, Lopes RD, et coll. Stroke and bleeding outcomes with apixaban versus warfarin in patients with high creatinine, low body weight or high age receiving standard dose apixaban for stroke prevention in atrial fibrillation. Eur Heart J 2015; 36(Supplément au résumé):345; et présenté par affiche au Congrès ESC 2015.
31. Ishak KJ, Phatak H, Rael M, et coll. A simulated head to head comparison of stroke and major bleeding with apixaban versus rivaroxaban in highrisk NVAF Patients. Eur Heart J 2015; 36(Supplément au résumé):743-4; et présenté par affiche au Congrès ESC 2015.
32. Hijazi Z, Lindback J, Ostlund O, et coll. External validation of the biomarker-based ABC-stroke risk score for atrial fibrillation. Eur Heart J 2015; 36(Supplément au résumé):710-1; et présenté par affiche au Congrès ESC 2015.
La préparation de cet article a été rendue possible grâce à un soutien de l’alliance Bristol-Myers Squibb/Pfizer. Les auteurs avaient une indépendance éditoriale complète pour la préparation de cet article et sont entièrement responsables de son exactitude. Le commanditaire n’a exercé aucune influence sur le choix du contenu ou sur le matériel publié.