

|
Mark Kirchhof, M.D., Ph. D., FRCPC Chef de la division de dermatologie
|

|
Loukia Mitsos, M.D., FRCPC Protoderma |
Le 30e congrès de l’European Academy of Dermatology and Venereology (EADV), qui s’est tenu virtuellement du 29 septembre ou 2 octobre 2021, a donné lieu à la présentation des plus récentes innovations en dermatologie et offert une plateforme propice aux échanges scientifiques approfondis. Afin de présenter les progrès scientifiques et les mises à jour de la pratique clinique, l’EADV a accueilli plus de 550 éminents conférenciers à l’occasion de la 30e édition de son congrès annuel et a élaboré un programme scientifique qui prévoyait dix conférences plénières et 160 séances de simulation en direct sur des sujets de pointe, les dernières nouvelles, des séances de communication gratuites, des affiches électroniques et des séances entre membres de l’industrie. Lors de ce congrès, la dermatite atopique (DA) a fait l’objet d’une couverture détaillée, de la physiopathologie aux différentes modalités de traitement.
En ce qui a trait au traitement, le thème central était l’introduction continue de nouveaux produits biologiques et d’inhibiteurs des protéines JAK1. Les comparaisons du baricitinib, de l’upadacitinib et de l’abrocitinib avec le dupilumab laissent entrevoir l’offre d’une vaste gamme d’options de traitement personnalisé2. Outre les effets physiques de la DA, plusieurs présentations ont exploré ses aspects psychosociaux et reconnu la nécessité pour les médecins de mieux comprendre les difficultés que vivent les enfants atteints de DA et leur famille au quotidien3. Voici certains des moments forts du programme du congrès cette année qui ouvrent la voie à l’amélioration de la qualité de vie des patients atteints de DA et de leurs proches.
LA DERMATITE ATOPIQUE EST UNE MALADIE SYSTÉMIQUE
Certains chercheurs ont réuni les théories intrinsèques et extrinsèques relatives à la dermatite atopique en incorporant les facteurs déclenchants environnementaux, les anomalies de la barrière cutanée, les caractéristiques du microbiome intestinal et les caractéristiques immunitaires internes pour une pathogenèse plus unifiée. Les visions de la DA comme une maladie inflammatoire chronique commencent à refléter la façon dont nous classons et nous abordons le psoriasis4. Il est intéressant de noter que, comparativement aux sujets témoins et aux patients atteints de psoriasis, l’activité immunitaire des patients atteints de DA au niveau du sang périphérique était plus élevée; on a notamment observé une élévation supérieure des taux de cytokines et de lymphocytes T activés dans le sang circulant4.
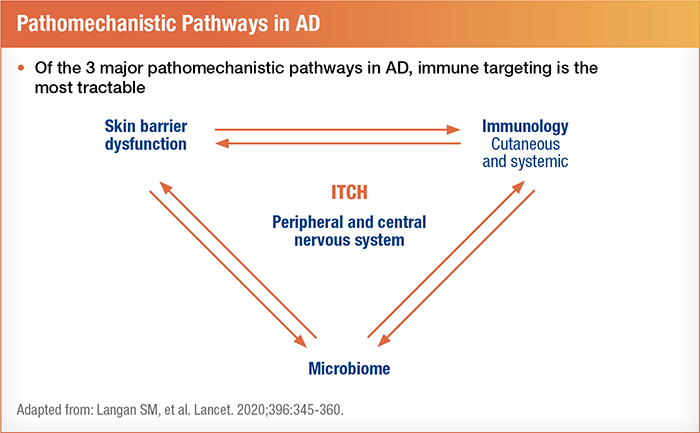
Le ciblage des voies de l’inflammation reconnues comme des options thérapeutiques dans d’autres maladies auto-immunes s’est révélé fructueux dans le traitement de la DA. Par exemple, une étude de phase II sur l’étrasimod (un modulateur sélectif des récepteurs de la sphingosine-1-phosphate par voie orale) a atténué de manière significative les symptômes de la DA chez plus de 100 participants après 12 semaines de traitement6. Les bonnes marges d’efficacité et d’innocuité de l’étrasimod ont déjà été établies dans le traitement de diverses affections, de la maladie de Crohn à l’alopécie en aires6.
La prise en charge de la DA sur le plan immunologique constitue une approche fructueuse et plusieurs autres traitements ciblés se sont révélés prometteurs. Des essais de phase II portant sur les anticorps monoclonaux qui ciblent l’axe OX40-OX40L, lequel pourrait intervenir à une étape précoce de la DA au niveau des voies de l’inflammation, laissent entrevoir une possible maîtrise de longue durée de la maladie1.
L’amlitélimab (KY1005) est un anticorps monoclonal ciblant le ligand d’OX40 (OX40L) de la famille des immunoglobulines G4 (IgG4), qui ne provoque pas la déplétion et qui cible les mécanismes de l’inflammation en amont; il est administré une fois par mois en monothérapie7. Les chercheurs ont mis sur pied 19 centres de recrutement répartis en Allemagne, en Pologne, en Grande-Bretagne et en Espagne afin d’évaluer son efficacité et sa marge d’innocuité. Les patients du groupe de traitement par l’amlitélimab à faible dose ont reçu une dose d’attaque de 200 mg suivie d’une dose d’entretien de 100 mg toutes les quatre semaines. Les patients du groupe de traitement par l’amlitélimab à forte dose ont reçu une dose d’attaque de 500 mg suivie d’une dose d’entretien de 250 mg toutes les quatre semaines. Les données de ces deux groupes ont été comparées avec celle du groupe témoin recevant un placebo.
Dans le cadre de cet essai, le traitement a été administré pendant les 12 premières semaines et les effets ont été observés à la 16e semaine (59 participants); un suivi de l’innocuité a été effectué à la 36e semaine (48 participants). On a observé une atténuation significative du prurit dans les deux groupes de traitement par l’amlitélimab, comparativement au placebo, de même que d’autres améliorations sur le plan des manifestations cutanées de la DA7. Même s’il y a lieu d’approfondir les recherches, cette recherche préliminaire appuie le concept qui sous-tend le ciblage d’OX40L à l’aide de médicaments comme l’amlitélimab pour le traitement des personnes atteintes de DA.
Une autre étude de phase II a examiné ce mécanisme à l’aide du KHK4083 (AMG 451). Cet anticorps monoclonal de la sous-classe des IgG1 stoppe l’expansion clonale des lymphocytes T et bloque la formation des lymphocytes T mémoires, ce qui inhibe les lymphocytes T activés, y compris les lymphocytes Th21. Les patients ont reçu soit 150 mg de KHK4083 par voie sous-cutanée toutes les quatre semaines, 300 mg toutes les deux semaines, 600 mg toutes les deux semaines ou 600 mg toutes les quatre semaines pendant toute la durée de l’étude de 36 semaines1. Au total, 273 participants de l’étude ont été répartis pour recevoir un placebo pendant 18 semaines avant de passer au KHK4083 administré par voie sous-cutanée à raison de 600 mg (toutes les deux semaines) au cours des semaines 18 à 36. Les résultats ont montré que le KHK4083 a atténué de manière significative les signes et les symptômes de la DA à la 16e semaine. De plus, les effets positifs associés au KHK4083 se sont maintenus pendant 20 semaines après l’arrêt du traitement; le traitement a été bien toléré et on n’a relevé aucune préoccupation significative sur le plan de l’innocuité1.
Les chercheurs ont également étudié une molécule à prise orale appelée RPT193, qui inhibe le récepteur de chimiokines 4 à motif (CCR4)8. Dans la DA, les lymphocytes Th2 s’accumulent dans la peau et expriment CCR4 de façon sélective, lequel est associé à des symptômes de DA plus sévères, incluant les démangeaisons. Au cours d’un essai de phase Ib, le RPT193 a atténué de manière significative les symptômes de la DA en 29 jours, comparativement au placebo, et a procuré des bienfaits qui se sont maintenus pendant deux semaines après l’arrêt du traitement8.
Une petite étude a également évalué les effets du spésolimab sur le dysfonctionnement de la barrière cutanée chez des patients atteints de DA. Le spésolimab est le premier anticorps monoclonal humanisé d’une sous-classe des IgG dirigé contre l’interleukine 36 qui a produit des améliorations cliniquement importantes (mais pas encore statistiquement significatives)9. Une cohorte de 51 participants adultes, de sexe masculin ou féminin, ont été répartis de façon aléatoire pour recevoir quatre injections de spésolimab (600 mg) ou d’un placebo, une fois toutes les quatre semaines. Les participants ayant obtenu un score EASI-75 ont été considérés comme ayant « répondu » au traitement; ils sont demeurés en observation pendant 12 semaines additionnelles sans poursuivre le traitement. Les sujets n’ayant « pas répondu » au traitement ont poursuivi le traitement par le spésolimab pendant 16 semaines supplémentaires. Les améliorations observées chez les sujets ayant répondu au traitement se sont maintenues jusqu’à la 28e semaine, malgré l’arrêt du traitement9. On n’a observé aucun effet indésirable marquant. Malheureusement, cette étude portait sur un très faible échantillon de cinq participants seulement10.
AUTRES TRAITEMENTS DE LA DA UTILISANT LES ANTICORPS MONOCLONAUX
Plusieurs autres anticorps monoclonaux sont en cours de développement, y compris un médicament expérimental appelé bermekimab, un inhibiteur du récepteur de l’IL-1α On pense que l’IL-1 accélère la réponse inflammatoire associée aux IL-13, IL-22 et IL-364. La quasi-totalité de cellules possède un récepteur de l’IL-1α laquelle est principalement sécrétée par les kératinocytes4. Des travaux de recherche antérieurs montrent qu’une déficience d’origine génétique de l’inhibiteur du récepteur de l’IL-1 entraîne une inflammation cutanée sévère à médiation immunitaire. De plus, on a observé une activation plus marquée de l’IL-1 dans les cellules cutanées d’adultes et d’enfants atteints de DA. Les résultats préliminaires d’une étude de phase II menée sans insu et portant sur l’administration de 400 mg de bermekimab semble indiquer que ce médicament entraîne une réponse rapide chez les patients atteints de DA4. Cependant, pour le moment, aucune étude comparative avec placebo n’a permis de valider ces résultats.
Des données plus solides sur le tralokinumab et le dupilumab émergent actuellement. Selon les données de recherche, chez les patients qui avaient répondu de manière satisfaisante au tralokinumab (un inhibiteur de l’IL-13) après 16 semaines, les bienfaits se seraient maintenus après 52 semaines lorsque le médicament était administré en traitement d’entretien toutes les deux semaines ou toutes les quatre semaines11. À plus long terme, une analyse des résultats de l’étude ECZTEND a été effectuée au bout de 2 ans dans une étude en cours de 5 ans sur le tralokinumab12. Au cours de ces deux années, 345 participants ont reçu des injections de 300 mg de tralokinumab toutes les deux semaines avec l’option d’inclure des corticostéroïdes topiques à l’issue de la phase d’attaque initiale à 600 mg. Certains participants avaient déjà été régulièrement traités par le tralokinumab dans le cadre d’études apparentées avant leur participation à cette étude. Chez les participants qui ne recevaient pas ce médicament avant de participer à l’étude, on a noté un degré de maîtrise des symptômes équivalent à celui des autres participants après 12 semaines de traitement. Les résultats ont montré des améliorations à long terme de la DA, y compris un sommeil de meilleure qualité et une atténuation des démangeaisons12.
Les études sur le dupilumab ont montré des améliorations pour ce qui est des anomalies de la barrière cutanée et des marqueurs de l’inflammation générale, ce qui consolide les théories selon lesquelles le ciblage de l’axe Th2 et des cytokines IL-4 et IL-13 pourrait renverser les manifestations de la DA4. Des bienfaits significatifs ont été documentés au cours des 2 semaines suivant l’instauration du traitement par le dupilumab. Qui plus est, les effets positifs observés après 16 semaines se sont maintenus jusqu’à la 52e semaine de la période d’observation5.
Dans le cadre d’une étude de prolongation ouverte sur le dupilumab à 300 mg, les résultats des participants ont été publiés après 172 semaines de traitement13. Ces analyses intérimaires ont porté sur les données hebdomadaires de 253 adultes (le traitement associait dans certains cas des traitements topiques) ayant participé à diverses études de phase I à III apparentées14. Les scores PP-NRS (Peak Pruritus Numerical Rating Scale), qui se situaient autour de 5 au départ, se sont rapidement améliorés au cours des 16 premières semaines de traitement, se stabilisant finalement à une valeur moyenne de 2,2 à l’issue des 172 semaines13. Comparativement aux valeurs initiales, on a observé une augmentation d’au moins 50 % des scores EASI chez 98,7 % des participants à la semaine 172. On a observé une amélioration de 75 % des scores EASI chez 94,6 % des participants et une amélioration de 90 % chez 82,6 % des participants14. De plus, le traitement de plus longue durée n’a soulevé aucune nouvelle préoccupation sur le plan de l’innocuité13.
DÉVELOPPEMENTS RELATIFS AUX PETITES MOLÉCULES INHIBITRICES DES KINASES JAK
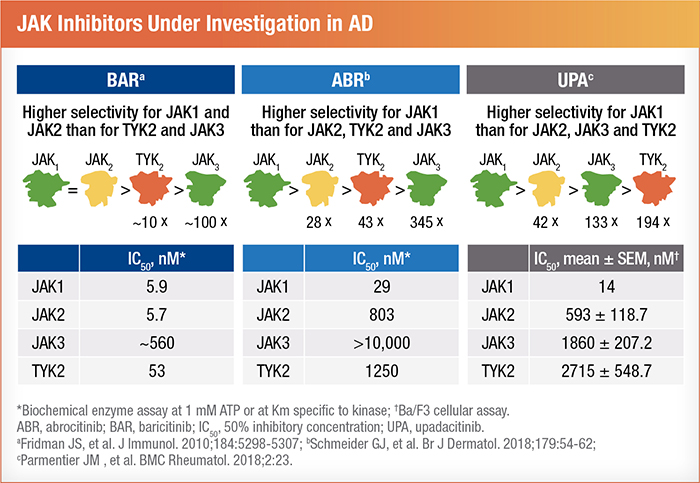
L’utilisation élargie du dupilumab a ouvert la voie à l’introduction d’inhibiteurs des protéines JAK plus récents dans des études comparatives. À l’heure actuelle, trois inhibiteurs des protéines JAK sont évalués dans le cadre d’études cliniques de phases avancées5. Au 4e trimestre de 2020, le baricitinib a été approuvé par l’Agence européenne des médicaments (EMA) et au Royaume-Uni (R.-U.). L’emploi de l’abrocitinib est autorisé chez les patients âgés de 12 ans ou plus au R.-U. et il est en cours d’évaluation aux États-Unis (É.-U.)15. Au Canada, l’upadacitinib est le seul inhibiteur des protéines JAK dont l’emploi est approuvé, mais il est toujours en cours d’évaluation en Europe et aux É.-U.5. Bien que ces trois médicaments visent la même cible, leur sélectivité varie en fonction des différentes voies5. En l’occurrence, le baricitinib a une sélectivité équivalente pour les protéines JAK 1 et JAK 2, alors que l’abrocitinib et l’upadacitinib ciblent principalement les protéines JAK 15. Nous avons bon espoir que ces variations quant à la sélectivité donneront lieu à des traitements efficaces et plus personnalisés de la DA4.
Les résultats de l’étude de phase III JADE COMPARE sur l’abrocitinib ont fait l’objet de discussions15. 15
Le graphique ci-dessous fournit un aperçu des modalités de cette étude :
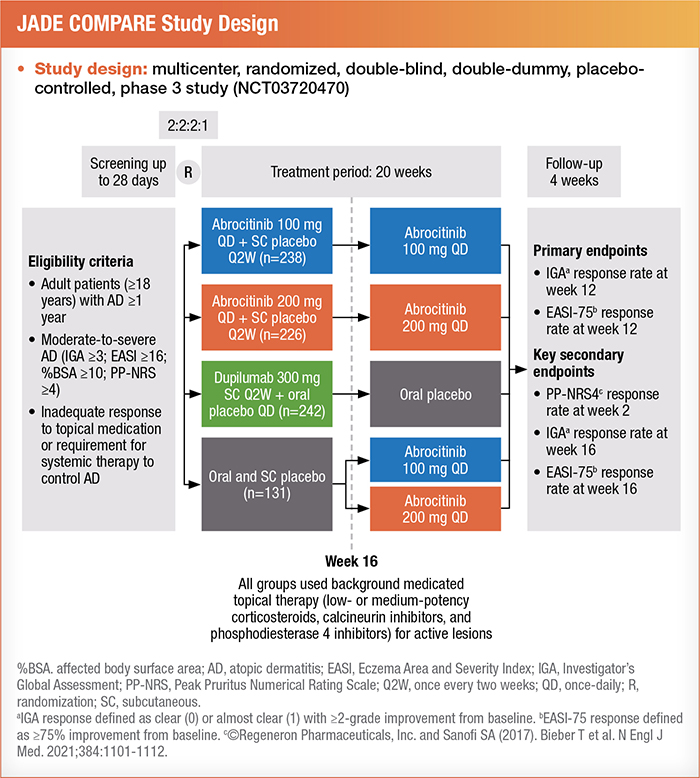
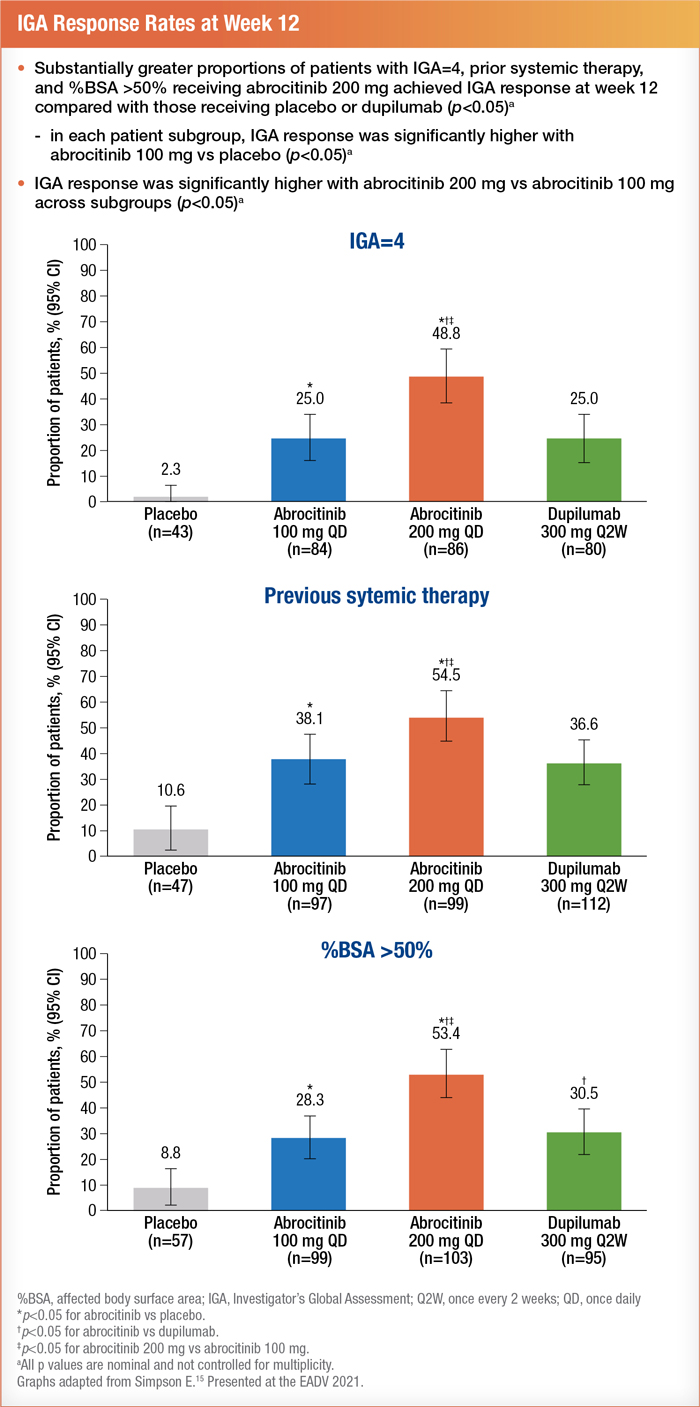
Les patients atteints d’une maladie sévère ont été répartis en trois sous-groupes, soit les patients qui avaient obtenu un score IGA de 4, ceux dont la surface corporelle touchée était > 50 % et ceux qui avaient déjà reçu un traitement immunosuppresseur à action générale (y compris des corticostéroïdes à action générale) pour le traitement de la DA15.
Les chercheurs ont analysé les données de 577 participants. L’efficacité du traitement a été mesurée au bout de 12 semaines par l’obtention d’un score IGA de 0 (disparition complète) ou de 1 (disparition quasi complète) en plus d’une amélioration ≥ 2 grades par rapport au début de l’étude ainsi qu’une amélioration ≥ 75 % du score EASI (réponse EASI-75)15. Les résultats ont montré que la dose de 200 mg d’abrocitinib constituait l’intervention la plus efficace, avec un résultat positif dans chaque sous-groupe. Les patients qui recevaient une dose quotidienne de 100 mg d’abrocitinib par voie orale ont obtenu des résultats comparables à ceux des patients qui recevaient une dose de 300 mg de dupilumab (administré par voie sous-cutanée toutes les deux semaines après une dose d’attaque de 600 mg)16.
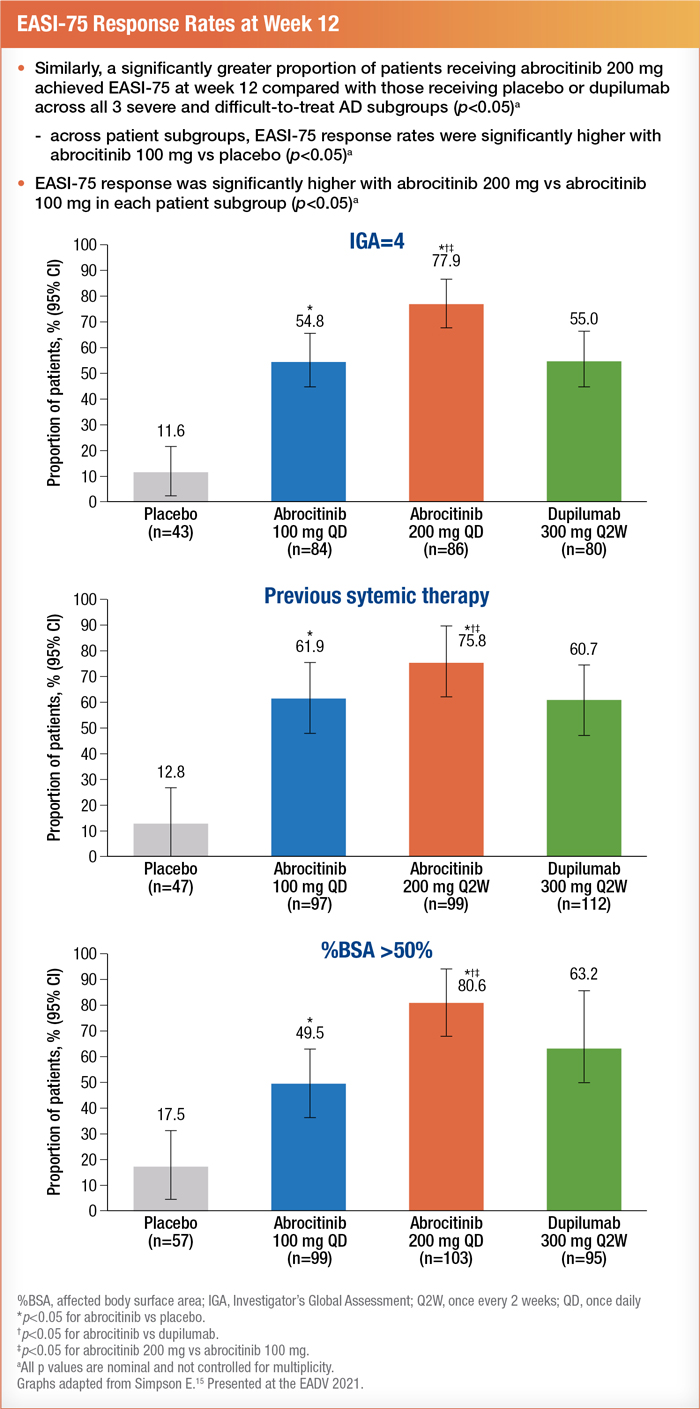
Les patients traités par l’abrocitinib ont bien toléré le traitement et aucune préoccupation n’a été soulevée sur le plan de l’innocuité15. Pour évaluer l’innocuité, les chercheurs ont analysé les effets indésirables survenus pendant le traitement (EISPT) − toutes causes confondues − et les EISPT graves. Parmi les 577 participants, 58,6 % ont signalé des EISPT de toutes causes et 2,1 %, des EISPT graves. Les effets indésirables les plus fréquemment associés à l’abrocitinib ont été la rhinopharyngite, les nausées, l’acné et les céphalées15.
L’abrocitinib a en outre été comparé au dupilumab dans le cadre d’une vaste étude de phase III de comparaison directe (JADE DARE) ayant englobé plus de 700 participants. Selon les résultats, on a observé une réponse rapide sur le plan des démangeaisons dans les deux semaines ayant suivi l’instauration du traitement par l’abrocitinib10. Voir ci-dessous :
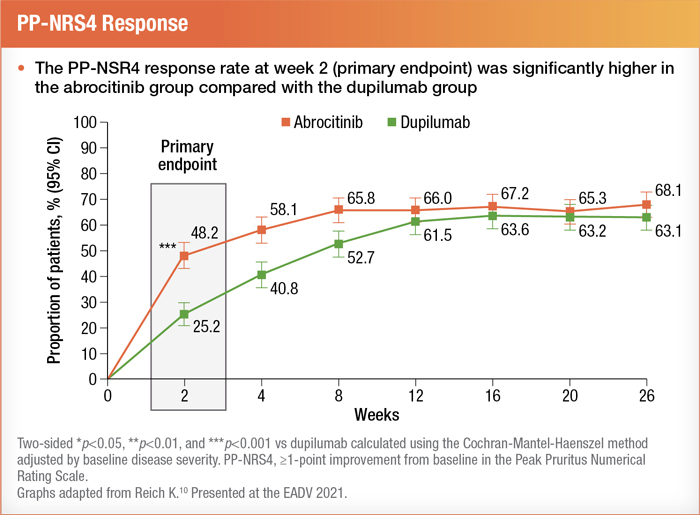
Qui plus est, les scores EASI-90 étaient significativement supérieurs après quatre semaines de traitement par l’abrocitinib et ils se sont maintenus pendant 16 semaines10.
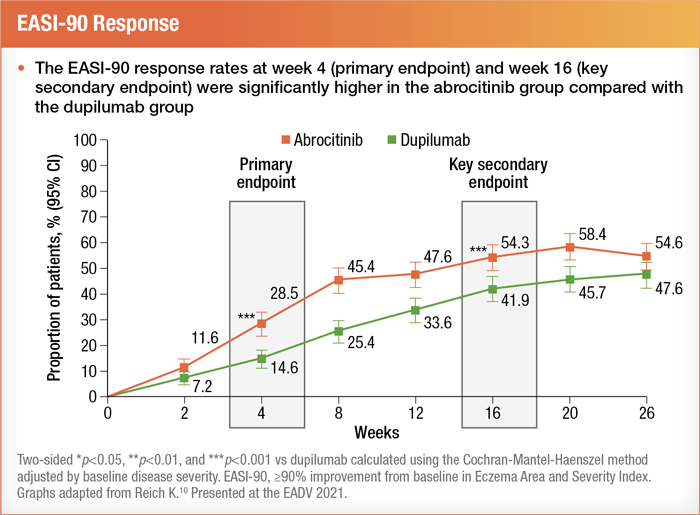
Durant l’étude, certains participants ont poursuivi leur traitement topique de fond. Dans sa présentation, le Dr Kristian Reich a néanmoins noté qu’on a observé « un plus grand nombre de jours sans corticostéroïdes avec un score EASI-90 avec l’abrocitinib, comparativement au dupilumab10 ». De plus, en ce qui a trait aux adolescents atteints de DA, l’étude de phase III JADE TEEN fournit un aperçu des données préliminaires selon lesquelles l’abrocitinib n’altère pas la réponse immunitaire des adolescents recevant le vaccin anticoquelucheux acellulaire (dcaT)17.
Le passage des patients traités par le dupilumab à l’upadacitinib a été évalué dans le cadre d’une étude de prolongation ouverte qui visait à comparer ces deux molécules18. Après la période initiale de six mois, tous les participants ont poursuivi leur traitement par l’upadacitinib pendant une période additionnelle de six mois. L’upadacitinib s’est révélé particulièrement bénéfique chez les patients qui n’avaient pas répondu au traitement par le dupilumab; 40 % des participants de ce deuxième groupe ont en effet obtenu une réponse EASI-100 après leur passage à l’upadacitinib18. Les améliorations ont commencé quatre semaines après la substitution et elles se sont maintenues jusqu’à la fin de l’étude.
L’upadacitinib a réduit de manière significative le prurit et d’autres paramètres de la DA18. Lors de la comparaison de quatre régions corporelles, les chercheurs ont conclu que le pourcentage de patients ayant obtenu une réponse EASI-75 était plus élevé dans le groupe upadacitinib que dans le groupe dupilumab, et ce dans toutes les régions corporelles. Ces résultats supérieurs ont été observés aussi tôt que la semaine 1 et se sont maintenus jusqu’à la semaine 16, comme indiqué ci-dessus19 :
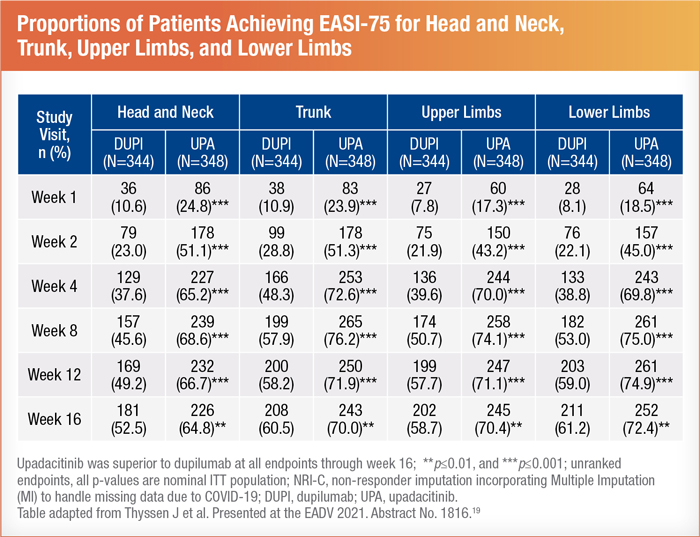
Les participants ont observé un repos thérapeutique de deux semaines entre les traitements afin de réduire au minimum les possibles effets résiduels du dupilumab. Conséquemment, on pense que l’upadacitinib à lui seul est à l’origine de la courbe d’amélioration abrupte, mais les chercheurs ont reconnu que certains effets mixtes pourraient être en cause18. Aucun nouveau problème d’innocuité associé à l’upadacitinib n’a été repéré. L’effet indésirable le plus notable a été l’acné d’intensité légère20. Après la présentation de ces résultats, des questions ont été posées quant à la marge d’innocuité de l’upadacitinib chez les patients ayant des antécédents de cancer. Toutefois, les chercheurs ont indiqué qu’ils ne disposaient pas de suffisamment de données à long terme pour offrir des conseils à cet égard18.
INHIBITEURS DES PROTÉINES JAK TOPIQUES
En plus des médicaments injectables et oraux, les inhibiteurs des JAK topiques sont également évalués à divers stades d’essais cliniques. Le delgocitinib en crème est un inhibiteur pan-JAK qui a été évalué dans le cadre d’une étude clinique de phase IIb sur les démangeaisons et la douleur liées à l’eczéma21. Au total, 258 adultes atteints d’eczéma chronique des mains ont été répartis au hasard dans cinq groupes; chaque participant avait la consigne d’appliquer la crème deux fois par jour. La teneur variait selon les crèmes : delgocitinib à 20 mg/g, à 8 mg/g, à 3 mg/g ou à 1 mg/g, ou un excipient en crème. Les participants qui utilisaient la crème ayant la teneur le plus élevée ont connu une atténuation statistiquement significative des démangeaisons et de la douleur au bout d’une semaine. Dans tous les groupes de traitement par le delgocitinib en crème, les améliorations ont été significativement supérieures à celles observées dans le groupe ayant reçu l’excipient en crème21.
Dans deux études de phase III sur le ruxolitinib en crème (qui est sélectif des protéines JAK 1 et JAK 2) les résultats se sont révélés positifs chez patients âgés de 65 ans ou plus, en particulier quant aux troubles du sommeil et au prurit22. Une étude à double insu de plus de deux ans a porté sur 1249 patients âgés de 12 ans ou plus répartis aléatoirement pour recevoir le ruxolitinib en crème à 0,75 %, le ruxolitinib en crème à 1,5 % ou un excipient en crème, deux fois par jour pendant huit semaines23. Une analyse de sous-groupe a englobé 114 adultes de plus de 65 ans. Les effets anti-inflammatoires et les améliorations relatives à la qualité de vie sont encourageants pour cette population sous-étudiée d’adultes plus âgés atteints de DA22. Les données de ces études appuient les bienfaits du ruxolitinib en crème observés antérieurement dans les études TRuE-AD23.
ASPECTS PSYCHOSOCIAUX DE LA DA CHEZ LES ENFANTS, LES SOIGNANTS ET LES PROFESSIONNELS DE LA SANTÉ
L’étude AD-GAP (Atopic Dermatitis - Global Adolescent & Pediatric) a évalué l’expérience qualitative et quantitative d’enfants et d’adolescents atteints de DA, de leurs parents ou soignants et de leur médecin. Les chercheurs ont repéré des distinctions importantes entre les perceptions des jeunes patients atteints de DA et des personnes qui participent à leurs soins3.
Le volet qualitatif de l’étude, qui s’est déroulé de mai à septembre 2020, a reposé sur de courts questionnaires, des entrevues exhaustives et des tests de réponse émotionnelle (images appropriées à l’âge des sujets pour engager la discussion sur les émotions) afin de recueillir des données de recherche sur les répercussions psychosociales de la DA sur les enfants et les adolescents3. De plus, les chercheurs ont évalué un échantillon de 72 soignants et de 72 médecins (incluant des pédiatres, des dermatologues et des allergologues). Plus tard, de mars à avril 2021, les chercheurs ont effectué le volet quantitatif de l’étude englobant 1447 patients, 1447 soignants et 1092 médecins, dont 45 % étaient des dermatologues3.
Les principales observations sont les suivantes :
- Les enfants et adolescents avaient tendance à se concentrer sur le présent.
- Les adolescents ont décrit leur affection comme étant douloureuse, marquée par les démangeaisons et gênante; ils ont indiqué qu’ils préféraient être seuls et qu’ils ne pouvaient pas participer à des activités qu’ils aiment.
- Les parents et les soignants se sont montrés préoccupés par l’avenir; incluant les possibles répercussions que la DA pourrait avoir sur leurs enfants au cours des années à venir, notamment sur leur carrière et leurs relations amoureuses.
- Lorsqu’on les a interrogés au sujet de leurs préoccupations à l’égard des effets indésirables du traitement, 68 % des soignants ont déclaré s’inquiéter des possibles répercussions du traitement de la DA sur leur enfant, et 63 % avaient peur que l’affection s’aggrave avec l’âge3.
- Les médecins ont fréquemment rapporté un faible degré d’observance thérapeutique et ont admis ne pas s’intéresser à la qualité de vie lors de chaque visite en raison d’obstacles liés aux contraintes de temps ou à l’évitement des sujets sensibles3.
Une discussion suscitant la réflexion à laquelle assistait le président, Korey Capozza, portait sur le point de vue d’un parent d’un adolescent atteint de DA24. Les stratégies pratiques destinées aux professionnels de la santé comprenaient les suivantes :
- Utiliser le temps passé dans la salle d’attente pour offrir des outils de sondage afin de générer des discussions plus approfondies durant les visites.
- Séparer les parents et les adolescents durant les visites pour court-circuiter les luttes de pouvoir et les dynamiques familiales improductives.
- Favoriser l’indépendance des jeunes patients et leur sens des responsabilités dans la prise en charge de la DA, en encourageant les adolescents et les enfants plus âgés à orienter la discussion et à participer à la prise de décision.
- S’assurer que les familles rencontrent toujours le même professionnel de la santé, si possible, pour créer un lien.
- Reconnaître le processus consistant à éliminer les vieux mécanismes d’adaptation à mesure que le traitement se montre efficace et transforme éventuellement la vie des patients.
L’inhibition des protéines JAK au-delà de la DA
Cette année, le congrès de l’EADV a aussi donné lieu à des discussions sur la façon dont les nouveaux inhibiteurs de protéines JAK constituent possiblement une option thérapeutique pour de multiples affections dermatologiques.
Par exemple, les données d’une étude multicentrique de phase II montrent des résultats prometteurs pour une petite molécule inhibitrice des protéines JAK, le jaktinib, dans le traitement de l’alopécie sévère25. Dans cet essai ouvert à 3 groupes, 111 adultes ont été répartis au hasard pour recevoir quotidiennement le jaktinib à 200 mg ou à 150 mg, ou le jaktinib à 50 mg 2 fois par jour. Dans tous les groupes, on a observé des bienfaits significatifs après 24 semaines. De plus, les doses plus faibles se sont révélées efficaces et ont entraîné moins d’effets indésirables, suggérant un excellent potentiel pour de futures études.
Les adultes atteints de vitiligo généralisé devraient garder un œil sur un inhibiteur des protéines JAK 3 et des kinases TEC pour la voie orale, le ritlecitinib (PF-06651600). Dans le cadre d’une étude de phase IIb englobant 364 patients adultes, ce médicament s’est révélé efficace et bien toléré, comparativement au placebo26. L’administration de différentes doses aux participants de six groupes de traitement a produit des améliorations continues au cours des 48 semaines de traitement. Toutefois, les changements les plus marqués ont été observés entre les semaines 24 et 48, alors que tous les participants ont reçu la dose la plus élevée de 200 mg de la semaine 24 à la semaine 28, suivie d’une dose d’entretien de 50 mg jusqu’à la semaine 4826.
CONCLUSIONS
Les patients atteints de DA disposent à présent d’autres options thérapeutiques, à mesure que les inhibiteurs des protéines JAK pour la voie orale, l’abrocitinib, le baricitinib et l’upadacitinib continuent d’être approuvés dans de nouveaux pays2. L’association de traitements nouveaux et plus anciens ne peut que contribuer à combler les besoins croissants des patients atteints de diverses affections inflammatoires, en dermatologie et dans d’autres domaines thérapeutiques. Comparativement aux trois articles publiés dans les années 1940, à l’heure actuelle, plus de 2000 études sur la DA ont été menées, et plus de 1000 essais sont en cours27. Le choix entre de nombreux médicaments oraux, crèmes topiques et traitements sous-cutanés outillera davantage les professionnels de la santé grâce à des traitements ciblés qui répondent aux besoins biologiques et aux enjeux liés au mode de vie de chaque patient28.
Sujets de réflexion :
1. En quoi les options de traitement de la dermatite atopique (DA) ont-elles changé? Qu’est-ce qui a déclenché la révolution dans ce domaine?
2. À votre avis, quelles pourraient être les répercussions du paradigme de traitement en évolution sur la façon dont nous prendrons en charge la DA et traiterons les patients qui en sont atteints à l’avenir?
3. Comment pouvons-nous maximiser l’emploi des traitements offerts actuellement à nos patients atteints de DA?
4. D’après les recherches et les données des d’études émergentes, où se situent les produits biologiques et les inhibiteurs des protéines JAK dans l’arsenal thérapeutique de la DA? Selon vous, quels sont les patients qui profiteraient le plus de ces traitements?
Références :
1. Guttman-Yassky E. Efficacy and safety results of KHK4083/AMG 451 (anti-OX40 mAb) in subjects with moderate to severe atopic dermatitis: a phase 2, multicentre, randomized, double-blind, parallel-group, placebo-controlled study. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : D3T01.1B.
2. Nezamololama N, Fieldhouse K, Metzger K, Gooderham M. Emerging systemic JAK inhibitors in the treatment of atopic dermatitis: a review of abrocitinib, baricitinib, and upadacitinib. Drugs in Context 2020; 9: 2020-8-5. DOI: 10.7573/dic.2020-8-5
3. Paller A. Addressing the full impact of AD. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : SAT 51.02.
4. Guttman-Yassky E. AD pathophysiology and role of IL-1α in AD. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : SAT 59.02.
5. Irvine A. Overview of therapeutic targets in AD. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : SAT 59.03.
6. Etrasimod, a novel, oral selective sphingosine 1-phosphate receptor modulator, in adults with moderate-to-severe atopic dermatitis: analysis of patient-reported outcomes and itch in a phase 2 clinical trial. Abrégé no 1293
7. Weidinger S. A Phase 2a study of KY1005, a novel non-depleting anti-OX40Ligand (OX40L) mAb in patients with moderate to severe AD. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : D1T01.3A.
8. Clinical safety and efficacy of RPT193, an oral CCR4 inhibitor: results from a randomized, placebo-controlled Phase 1b monotherapy trial in patients with moderate-to-severe atopic dermatitis. Abrégé no 2746
9. Bissonnette R. Efficacy and safety of spesolimab, an anti-interleukin-36 receptor antibody, in patients with moderate-to-severe atopic dermatitis. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : FC01.06.
10. Reich K. Efficacy and safety of abrocitinib versus dupilumab in adults with moderate-to-severe atopic dermatitis who received background topical therapy in a 26-week, randomized, head-to-head trial. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : D3T01.2B.
11. Predictors of maintained response with tralokinumab every four weeks dosing in adults with moderate-to-severe atopic dermatitis. Abrégé no 2948
12. Blauvelt A. Two-year maintenance of response with tralokinumab in moderate-to-severe atopic dermatitis: Interim analysis of the ECZTEND open-label extension trial. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : FC01.04.
13. Bruin‑Weller M. Long-term efficacy of dupilumab in adults with moderate-to-severe atopic dermatitis: Results from an open-label extension trial up to 172 weeks. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : FC01.02.
14. Long-term efficacy of dupilumab in adults with moderate-to-severe atopic dermatitis: results from an open-label extension trial up to 172 weeks. Abrégé no 2008
15. Simpson E. Efficacy of abrocitinib in severe and difficult-to-treat patients with moderate-to-severe atopic dermatitis in the phase 3 JADE COMPARE study. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : FC01.05.
16. Efficacy of abrocitinib in severe and difficult-to-treat patients with moderate-to-severe atopic dermatitis in the phase 3 JADE COMPARE study. Abrégé no 1024
17. The impact of abrocitinib on vaccine-induced immune responses in adolescents with moderate-to-severe atopic dermatitis undergoing routine tetanus, diphtheria, and pertussis vaccination in phase 3 JADE TEEN. Abrégé no 794
18. Blauvelt A. Efficacy and safety of switching from dupilumab to upadacitinib in moderate-to-severe atopic dermatitis: results from an open label extension trial. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : D1T01.3B.
19. Efficacy and safety of upadacitinib vs dupilumab treatment for moderate to severe atopic dermatitis in four body regions - analysis from the Heads Up study. Abrégé no 1816
20. Thyssen J. Efficacy and safety of upadacitinib vs dupilumab treatment for moderate to severe atopic dermatitis in four body regions - Analysis from the Heads Up study. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : FC01.03.
21. Agner T. The topical pan-JAK inhibitor delgocitinib in a cream formulation reduces itch and pain in chronic hand eczema. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : FC06.05.
22. Szepietowski J. Efficacy and safety of ruxolitinib cream among patients aged ≥65 years with atopic dermatitis: Pooled results from two phase 3 studies. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : FC01.01.
23. Efficacy and safety of ruxolitinib cream among patients aged ≥65 years with atopic dermatitis: pooled results from two phase 3 studies. Abrégé no 1092
24. Capozza K, et al. Living in the now with AD: panel discussion. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : SAT 51.03.
25. Jaktinib, a novel JAK inhibitor in treatment of patients with severe alopecia areata: a randomized, three-arm, open-label and multicenter phase II dose-ranging study. Abrégé no 2499
26. Efficacy and safety of the oral Janus kinase 3/TEC inhibitor ritlecitinib (PF06651600) in adults with active non-segmental vitiligo: results from a phase 2b, randomized, dose-ranging study with an extension period. Abrégé no 2850
27. Langley R. Biologics and small molecules for atopic dermatitis. Présentation lors du congrès de l’EADV de 2021; identification de la présentation : D2T01.4C.
28. Salvati L, Cosmi L, Annunziato F. From emollients to biologicals: targeting atopic dermatitis. IJMS. 2021;22(19):10381. DOI: 10.3390/ijms221910381
Cette ressource d’apprentissage a été rendue possible grâce à une contribution à visée éducative de Pfizer Canada inc. Le contenu de cette ressource et les opinions qui y sont exprimées sont ceux des participants et elles ne représentent pas nécessairement celles des éditeurs ou du commanditaire. Les médecins doivent consulter les monographies autorisées par les instances fédérales avant de poser un diagnostic ou d’instaurer un traitement en fonction des recommandations formulées dans le présent document.