
Question 1 : Dans quelle mesure le taux d’HbA1c du patient influe-t-il sur le choix entre un inhibiteur de la DPP-4 ou un inhibiteur du SGLT2 comme traitement antihyperglycémiant d’appoint?
Question 2 : Quelle est l’importance de l’âge dans le choix d’un traitement antihyperglycémiant d’appoint?
Introduction
La metformine est l’antihyperglycémiant de première intention recommandé dans les lignes directrices pour le traitement du diabète de type 2 au Canada1. Chez les patients qui ne parviennent pas à atteindre leur valeur cible d’HbA1c avec la metformine, les Lignes directrices de pratique clinique 2018 de Diabète Canada recommandent un traitement d’appoint choisi en fonction des caractéristiques de chaque patient. On y retrouve également des recommandations claires concernant le traitement des patients atteints de diabète de type 2 présentant une maladie cardiovasculaire (CV) clinique, à savoir l’ajout de l’un des trois agents suivants aux bénéfices cardiovasculaires démontrés : l’empagliflozine, le liraglutide ou la canagliflozine1. Chez les patients exempts de maladie CV, les lignes directrices privilégient l’administration d’un inhibiteur de la DPP-4, d’un agoniste des récepteurs du GLP 1 ou d’un inhibiteur du SGLT2, si la priorité est d’éviter une hypoglycémie et/ou un gain de poids.
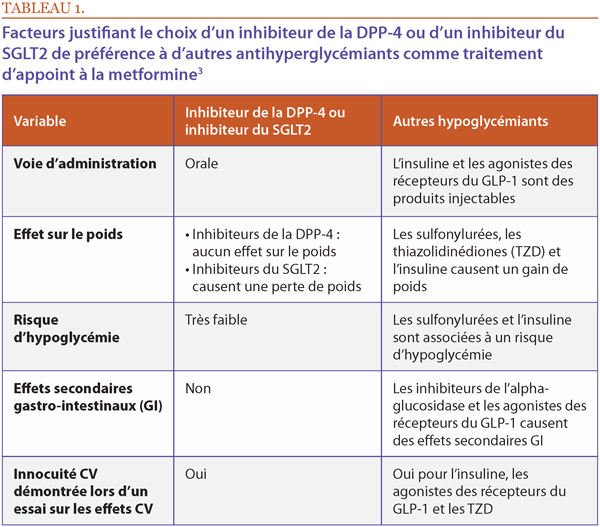
Dans les recommandations de l’American Association of Endocrinologists et de l’American College of Endocrinology, les agonistes des récepteurs du GLP-1 figurent en tête de liste des traitements d’appoint à la metformine, suivis des inhibiteurs du SGLT2 et des inhibiteurs de la DPP-4, qui sont les traitements d’appoint privilégiés par voie orale2. Comme l’indique le Tableau 1, plusieurs facteurs importants justifient le recours à des agents oraux, tels les inhibiteurs du SGLT2 ou de la DPP-43.
Dans cette revue, je répondrai à d’importantes questions sur des variables clés pouvant aider les cliniciens et leurs patients à choisir entre les inhibiteurs de la DPP-4 et les inhibiteurs du SGLT2 ou à opter pour les deux dans le traitement antihyperglycémiant d’appoint par voie orale du diabète de type 2 en l’absence de maladie CV.
Question 1 : Dans quelle mesure le taux d’HbA1c du patient influe-t-il sur le choix entre un inhibiteur de la DPP-4 ou un inhibiteur du SGLT2 comme traitement antihyperglycémiant d’appoint?
Réponse : Des méta-analyses ayant évalué la diminution du taux d’HbA1c associée à l’ajout d’un inhibiteur de la DPP-4 ou d’un inhibiteur du SGLT2 au traitement par la metformine ne montrent aucune différence significative entre ces deux classes de médicaments ou n’indiquent qu’une faible différence (0,11 %-0,17 %) en faveur des inhibiteurs du SGLT24-6.
Bien qu’aucune recommandation concluante ne puisse être formulée à partir de ces résultats globaux, ceux-ci permettent néanmoins d’énoncer quelques observations importantes quant à l’efficacité glycémique en fonction du taux initial d’HbA1c3. Même si aucune étude n’a stratifié les patients de manière prospective d’après leur taux initial d’HbA1c pour comparer l’efficacité des inhibiteurs de la DPP-4 et des inhibiteurs du SGLT2 à diminuer le taux d’HbA1c, des analyses par sous-groupes a posteriori montrent que l’efficacité des inhibiteurs du SGLT2 est supérieure à celle des inhibiteurs de la DPP-4 chez les patients dont le taux initial d’HbA1c est élevé (≥ 8 à 8,5 %), alors que les inhibiteurs de la DPP-4 ont procuré des avantages numériquement supérieurs par rapport aux inhibiteurs du SGLT2 chez les patients qui avaient au départ un taux d’HbA1c se situant à l’extrémité inférieure de la fourchette (< 8 à 8,5 %) (Figure 1)7,8.
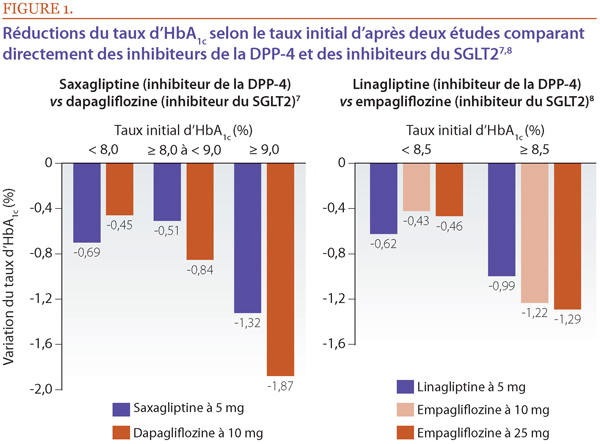
Ces résultats portent à croire qu’il pourrait être raisonnable de privilégier un inhibiteur du SGLT2 plutôt qu’un inhibiteur de la DPP-4 chez les patients dont le taux d’HbA1c s’éloigne davantage de la valeur cible malgré un traitement par la metformine. À l’inverse, les patients dont le taux initial d’HbA1c est moins élevé pourraient bénéficier davantage de l’ajout d’un inhibiteur de la DPP-4 que d’un inhibiteur du SGLT2.
Il convient toutefois de souligner que, bien qu’un traitement d’appoint par un inhibiteur du SGLT2 puisse être préférable à un traitement par un inhibiteur de la DPP-4 pour réduire le taux d’HbA1c chez les patients dont le taux initial est passablement élevé, les données probantes montrent que l’association de ces deux agents (avec la metformine) est significativement plus efficace pour réduire le taux d’HbA1c et augmente la probabilité d’atteindre la valeur cible d’HbA1c, comparativement à l’ajout de l’un ou l’autre de ces agents. Trois études distinctes ont évalué la réduction du taux d’HbA1c obtenue avec l’ajout d’une ou de ces deux classes de médicaments au traitement par la metformine7-9. Dans chacune de ces études, les patients ayant reçu un agent de chacune de ces classes, en plus de la metformine, ont été beaucoup plus susceptibles d’atteindre leur taux cible d’HbA1c que ceux ayant reçu un seul de ces deux agents. Dans ces trois études, la proportion de patients qui présentaient un taux initial d’HbA1c allant de 8,0 % à 8,9 % et qui ont réussi à atteindre un taux < 7,0 % a varié de 41 % à 62 % chez les patients ayant reçu les deux agents en association, alors qu’elle a été de 18 % à 36 % chez les patients traités par un inhibiteur de la DPP-4 en monothérapie et de 22 % à 33 % chez ceux recevant un inhibiteur du SGLT2 en monothérapie. Dans une de ces études, 58 % des patients dont le taux initial d’HbA1c était < 8,0 % ont atteint un taux d’HbA1c < 7,0 % après un traitement d’appoint par un inhibiteur de la DPP-4, contre seulement 42 % après un traitement d’appoint par un inhibiteur du SGLT2. Cependant, au plus 19 % des patients ayant un taux initial d’HbA1c ≥ 8,0 % ont atteint leur taux cible d’HbA1c après un traitement d’appoint par un inhibiteur de la DPP-4 ou un inhibiteur du SGLT2, alors que 50 % des sujets ayant un taux initial d’HbA1c de 8,0 % à < 9,0 % et 24 % des sujets ayant un taux initial d’HbA1c ≥ 9,0 % ont atteint leur valeur cible après avoir reçu ces deux traitements d’appoint en association7. Il y aurait donc lieu d’envisager un traitement d’appoint par un inhibiteur de la DPP-4 lorsque le taux d’HbA1c est < 8,0 %, mais il faudrait privilégier un traitement d’appoint associant un inhibiteur de la DPP-4 et un inhibiteur du SGLT2 lorsque le taux initial d’HbA1c est ≥ 8,0 %.
Question 2 : Quelle est l’importance de l’âge dans le choix d’un traitement antihyperglycémiant d’appoint?
Réponse : D’abondantes données probantes semblent indiquer que l’âge du patient est un facteur utile pour choisir entre un inhibiteur de la DPP-4 et un inhibiteur du SGLT2 comme traitement d’appoint à la metformine. Selon plusieurs études différentes, la réduction prévue du taux d’HbA1c associée aux inhibiteurs de la DPP-4 varie peu, qu’il s’agisse d’adultes âgés ou jeunes (réduction ajustée en fonction du placebo d’environ 0,6 % à 0,7 % chez les patients âgés de 65 ans et plus présentant un taux initial d’HbA1c d’environ 8,0 %)10-13. De plus, les effets secondaires des inhibiteurs de la DPP-4 dans la population âgée sont relativement bénins; le profil d’effets secondaires est d’ailleurs pratiquement impossible à distinguer de celui associé au placebo.
À l’inverse, l’efficacité des inhibiteurs du SGLT2 à abaisser le taux d’HbA1c semble moindre chez les patients âgés que chez les plus jeunes14,15. Ainsi, les réductions approximatives du taux d’HbA1c ajustées en fonction du placebo varient de 0,4 à 0,6 % avec ces agents chez les patients de 65 ans et plus. Selon certains, ces effets seraient dus à deux facteurs principaux, à savoir les taux initiaux d’HbA1c moins élevés chez les patients âgés inclus dans les essais cliniques et la réduction du débit de filtration glomérulaire estimé (DFGe) dans les cohortes âgées par rapport aux plus jeunes. Les patients âgés pourraient également être plus sujets aux effets secondaires liés au volume qui découlent de l’inhibition du SGLT2.
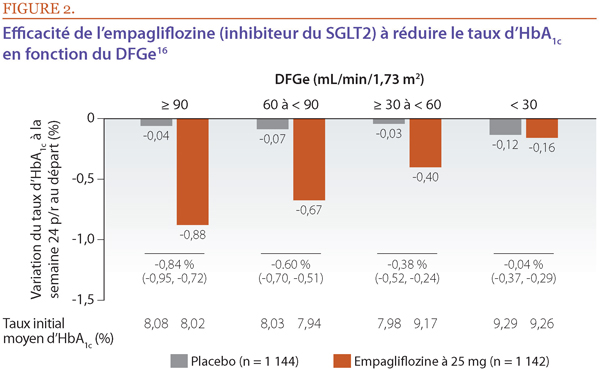
La fonction rénale est un important facteur à prendre en compte dans la prise en charge des patients atteints de diabète de type 2, car environ 40 % d’entre eux présentent également une néphropathie chronique. Il a ainsi été démontré que la fonction rénale, mesurée par le DFGe, est un facteur prédictif de l’effet réducteur des inhibiteurs du SGLT2 sur le taux d’HbA1c, la réduction du taux d’HbA1c étant moins marquée chez les patients ayant un DFGe plus faible (fonction rénale réduite) que chez ceux dont la fonction rénale est normale (Figure 2)16. Ces résultats s’expliquent par le fait que l’efficacité des inhibiteurs du SGLT2 à abaisser le taux d’HbA1c dépend du degré de glycosurie; chez les patients traités par des inhibiteurs du SGLT2, la glycosurie diminue à mesure que le DFGe diminue, ce qui a pour effet de réduire l’efficacité antihyperglycémiante. Les patients atteints d’insuffisance rénale modérée qui sont traités par un inhibiteur du SGLT2 pourraient également présenter plus d’effets indésirables liés au volume (p. ex. hypotension).
À l’inverse, des études cliniques évaluant des inhibiteurs de la DPP-4 chez des patients présentant une insuffisance rénale démontrent une efficacité et une innocuité comparables à celles observées chez les patients dont la fonction rénale est normale17. Fait à noter, l’alogliptine, la saxagliptine et la sitagliptine, des inhibiteurs de la DPP-4, sont excrétées par voie rénale, et les études pharmacocinétiques démontrent une exposition au médicament plus élevée chez les patients atteints d’insuffisance rénale modérée ou grave. Il faut donc administrer des doses plus faibles à ces patients. Cette « posologie rénale » est un problème d’ordre pharmacocinétique et n’est pas issue de préoccupations relatives à l’efficacité ou à l’innocuité; les inhibiteurs de la DPP-4 ne sont pas considérés comme néphrotoxiques.
Les lignes directrices de Diabète Canada et les monographies de produit fournissent des recommandations précises sur l’utilisation des inhibiteurs du SGLT2 et de la DPP-4 chez les patients dont la fonction rénale est réduite1. La canagliflozine ne devrait pas être administrée aux patients dont le DFGe est < 60 mL/min. Si le DFGe baisse sous le seuil de 60 mL/min, le traitement par la canagliflozine peut être poursuivi à une dose de 100 mg, mais il devient contre-indiqué à un DFGe < 45 mL/min. La canagliflozine peut toutefois être envisagée à des fins de protection CV et rénale chez les patients dont le DFGe est > 30 mL/min et qui présentent une maladie CV clinique, selon Diabète Canada1. La dapagliflozine est contre-indiquée chez les patients dont le DFGe est < 60 mL/min. La monographie de produit mise à jour de l’empagliflozine permet l’instauration de ce traitement lorsque le DFGe est ≥ 30 mL/min, mais précise que cet agent est contre-indiqué chez les patients présentant un DFGe < 30 mL/min18. Ainsi qu’il a été mentionné précédemment, les inhibiteurs de la DPP-4 peuvent être utilisés sans danger chez les patients présentant une insuffisance rénale. La linagliptine (non excrétée par voie rénale) peut être prescrite à la dose habituelle de 5 mg, mais doit être utilisée avec prudence chez les patients présentant une néphropathie terminale, en raison des données cliniques limitées. Un ajustement de la posologie de l’alogliptine, de la saxagliptine et de la sitagliptine est nécessaire en présence d’une insuffisance rénale modérée ou grave. La saxagliptine n’est pas recommandée chez les patients présentant une néphropathie terminale, tandis que l’alogliptine et la sitagliptine peuvent être utilisées à des doses de 6,25 mg et de 25 mg, respectivement.
Ces observations sur l’efficacité et l’innocuité laissent croire qu’il est raisonnable de recommander un inhibiteur de la DPP-4 de préférence à un inhibiteur du SGLT2 comme traitement d’appoint chez les patients âgés exempts de maladie CV qui sont atteints de diabète de type 2 et qui n’arrivent pas à atteindre leur taux cible d’HbA1c malgré la prise de metformine en monothérapie.
Références :
1. Lipscombe L, Booth G, Butalia S, et coll. Diabetes Canada 2018 clinical practice guidelines for the prevention and management of diabetes in Canada: pharmacologic glycemic management of type 2 diabetes in adults. Can J Diabetes 2018; 42(Suppl 1):S88-S103.
2. Garber AJ, Abrahamson MJ, Barzilay JI, et coll. Consensus statement by the American Association of Clinical Endocrinologists and American College of Endocrinology on the comprehensive type 2 diabetes management algorithm – 2018 executive summary. Endocr Pract 2018; 24(1):91-121.
3. Goldenberg RM. Choosing dipeptidyl peptidase-4 inhibitors, sodium-glucose cotransporter-2 inhibitors, or both, as add-ons to metformin: patient baseline characteristics are crucial. Clin Ther 2017; 39(12):2438-47.
4. Mishriky BM, Tanenberg RJ, Sewell KA, et coll. Comparing SGLT-2 inhibitors to DPP-4 inhibitors as an add-on therapy to metformin in patients with type 2 diabetes: A systematic review and meta-analysis. Diabetes Metab 2018; 44(2):112-20.
5. Wang Z, Sun J, Han R, et coll. Efficacy and safety of sodium-glucose cotransporter-2 inhibitors versus dipeptidyl peptidase-4 inhibitors as monotherapy or add-on to metformin in patients with type 2 diabetes mellitus: a systematic review and meta-analysis. Diabetes Obes Metab 2018; 20(1):113-20.
6. Maruthur NM, Tseng E, Hutfless S, et coll. Diabetes mmedications as monotherapy or metformin-based combination therapy for type 2 diabetes: a systematic review and meta-analysis. Ann Intern Med 2016; 164:740-51.
7. Rosenstock J, Hansen L, Zee P, et coll. Dual add-on therapy in type 2 diabetes poorly controlled with metformin monotherapy: a randomized double-blind trial of saxagliptin plus dapagliflozin addition versus single addition of saxagliptin or dapagliflozin to metformin. Diabetes Care 2015; 38:376-83.
8. DeFronzo RA, Lewin A, Patel S, et coll. Combination of empagliflozin and linagliptin as second-line therapy in subjects with type 2 diabetes inadequately controlled on metformin. Diabetes Care 2015; 38:384-93.
9. Pratley RE, Eldor R, Raji A, et coll. Ertugliflozin plus sitagliptin versus either individual agent over 52 weeks in patients with type 2 diabetes mellitus inadequately controlled with metformin: The VERTIS FACTORIAL randomized trial. Diabetes Obes Metab 2018; 20(5):1111-20.
10. Barnett AH, Huisman H, Jones R, et coll. Linagliptin for patients aged 70 years or older with type 2 diabetes inadequately controlled with common antidiabetes treatments: a randomised, double-blind, placebo-controlled trial. Lancet 2013; 382:1413-23.
11. Barzilai N, Guo H, Mahoney EM, et coll. Efficacy and tolerability of sitagliptin monotherapy in elderly patients with type 2 diabetes: a randomized, double-blind, placebo-controlled trial. Curr Med Res Opin 2011; 27:1049-58.
12. Doucet J, Chacra A, Maheux P, et coll. Efficacy and safety of saxagliptin in older patients with type 2 diabetes mellitus. Curr Med Res Opin. 2011; 27:863-9.
13. Pratley RE, McCall T, Fleck PR, et coll. Alogliptin use in elderly people: a pooled analysis from phase 2 and 3 studies. J Am Geriatr Soc 2009; 57:2011-9.
14. Bode B, Stenlof K, Harris S, et coll. Long-term efficacy and safety of canagliflozin over 104 weeks in patients aged 55-80 years with type 2 diabetes. Diabetes Obes Metab 2015; 17:294-303.
15. Leiter LA, Cefalu WT, de Bruin TW, et coll. Dapagliflozin added to usual care in individuals with type 2 diabetes mellitus with pre-existing cardiovascular disease: a 24-week, multicenter, randomized, double-blind, placebo-controlled study with a 28-week extension. J Am Geriatr Soc 2014; 62:1252-62.
16. Cherney DZ, Cooper ME, Tikkanen I, et coll. Pooled analysis of Phase III trials indicate contrasting influences of renal function on blood pressure, body weight, and HbA1c reductions with empagliflozin. Kidney Int 2018; 93(1):231-44.
17. Davis TM. Dipeptidyl peptidase-4 inhibitors: pharmacokinetics, efficacy, tolerability and safety in renal impairment. Diabetes Obes Metab 2014; 16(10):891-9.
18. Monographie de JARDIANCE. Boehringer Ingelheim (Canada) Ltée (16 avril 2018).
Le développement de cet article a été rendu possible grâce au soutien financier de Merck Canada Inc. Les opinions qui y sont exprimées sont celles de l’auteur et ne reflètent pas nécessairement les points de vue et les opinions de Merck Canada Inc. ou de STA HealthCare Communications inc. L’auteur a bénéficié d’une indépendance éditoriale complète pour l’élaboration du présent article et est responsables de son exactitude. Le commanditaire n’a exercé aucune influence sur la sélection du contenu ou du matériel publié.